
Wetenschap
Wat zijn de principes die betrokken zijn bij kristallisatie?
1. Supersaturation:
* De drijvende kracht: Kristallisatie treedt op wanneer een oplossing oververzadigd wordt, wat betekent dat deze meer opgeloste opgeloste stof bevat dan deze normaal kan vasthouden bij een gegeven temperatuur en druk. Deze toestand is onstabiel en de overtollige opgeloste stoffen wil uit oplossing komen en een vaste kristalfase vormen.
* Supersaturation creëren: Dit kan op verschillende manieren worden bereikt:
* Een hete oplossing afkoelen: Naarmate de temperatuur daalt, neemt de oplosbaarheid van de meeste vaste stoffen af, wat leidt tot oververzadiging.
* Verdamping: Het verwijderen van oplosmiddel uit een oplossing verhoogt de concentratie van de opgeloste stof en drijft deze naar oververzadiging.
* Een tweede oplosmiddel toevoegen: Het mengen van een oplossing met een oplosmiddel waarin de opgeloste stof minder oplosbaar is, kan neerslag veroorzaken.
* Chemische reacties: Reacties die een solide product produceren, kunnen leiden tot oververzadiging.
2. Nucleatie:
* De eerste stap: Nucleatie is de vorming van de eerste kleine, stabiele kristalkernen in de oververzadigde oplossing. Deze kernen werken als zaden voor verdere kristalgroei.
* Homogeen versus heterogene nucleatie:
* Homogeen: Nucleatie vindt spontaan plaats in de oplossing zelf. Vereist een hoge mate van oververzadiging.
* heterogeen: Nucleatie vindt plaats op het oppervlak van onzuiverheden of vreemde deeltjes in de oplossing. Vereist een lagere mate van oververzadiging.
* Controlerende nucleatie: Zorgvuldige controle over supersaturatie en onzuiverheden is cruciaal voor het produceren van kristallen met een gewenste grootte en uniformiteit.
3. Crystal Growth:
* toevoegen aan de kernen: Zodra kernen zijn gevormd, beginnen ze opgeloste moleculen aan te trekken en ze in hun kristalrooster op te nemen.
* Layer-by-Layer groei: Kristalgroei is een laag-voor-laag proces, waarbij nieuwe moleculen zich op een specifieke en geordende manier aan het bestaande kristaloppervlak hechten.
* factoren die de groei beïnvloeden:
* supersaturatieniveau: Hogere oververzadiging leidt tot snellere groei, maar kan ook leiden tot minder perfecte kristallen.
* Temperatuur: Temperatuur beïnvloedt de diffusiesnelheid en de oplosbaarheid van de opgeloste stof, waardoor de groei wordt beïnvloed.
* onzuiverheden: Onzuiverheden kunnen de kristalgroei verstoren en leiden tot defecten of onregelmatigheden.
4. Kristalgewoonte:
* Vorm is belangrijk: De externe vorm of gewoonte van een kristal wordt bepaald door de opstelling van atomen of moleculen in het kristalrooster.
* factoren die de gewoonte beïnvloeden:
* kristalstructuur: De inherente opstelling van atomen of moleculen in het kristalrooster dicteert de algehele vorm.
* Groeiomstandigheden: Temperatuur, oververzadigde niveau en de aanwezigheid van onzuiverheden kunnen allemaal de kristalgewoonte beïnvloeden.
5. Crystal Perfection:
* Niet altijd perfect: Kristallen kunnen onvolkomenheden hebben, bekend als defecten, die kunnen voortvloeien uit verschillende factoren zoals groeiomstandigheden, onzuiverheden of roosterspanning.
* Belang van perfectie: Kristalperfectie kan de fysische en chemische eigenschappen van het materiaal aanzienlijk beïnvloeden, waardoor de sterkte, geleidbaarheid of reactiviteit van invloed is.
Sleuteltoepassingen:
* Farmaceutische productie: Kristallisatie wordt gebruikt om actieve farmaceutische ingrediënten te zuiveren en te isoleren.
* chemische industrie: Kristallisatie wordt gebruikt om een breed scala aan chemicaliën te scheiden en te zuiveren.
* Materiaalwetenschap: Kristallisatie wordt gebruikt om materialen te creëren met specifieke eigenschappen voor elektronica, optica en andere velden.
Door deze principes te begrijpen, kunnen wetenschappers en ingenieurs het kristallisatieproces manipuleren en regelen om kristallen te creëren met gewenste eigenschappen voor specifieke toepassingen.
 Waarom wordt waterstof in de eerste groep geplaatst als het een niet -metaal is?
Waarom wordt waterstof in de eerste groep geplaatst als het een niet -metaal is?  Wat zou het totale potentieel zijn voor 3Ag2S 2Al(s) -- Al2S3 6Ag(s)?
Wat zou het totale potentieel zijn voor 3Ag2S 2Al(s) -- Al2S3 6Ag(s)?  In legeringen met vormgeheugen, de juiste combinatie van kristalkorrels kan een hoge sterkte bereiken en toch geheugen behouden
In legeringen met vormgeheugen, de juiste combinatie van kristalkorrels kan een hoge sterkte bereiken en toch geheugen behouden Welk type binding vormt zich tussen barium en zuurstof?
Welk type binding vormt zich tussen barium en zuurstof?  Is het mengen van een drankje in water fysiek of chemisch?
Is het mengen van een drankje in water fysiek of chemisch?
 Australië zal waarschijnlijk tot 35% meer El Niño's ervaren volgens nieuwe projecties
Australië zal waarschijnlijk tot 35% meer El Niño's ervaren volgens nieuwe projecties Een van Europa's ergste hongersnoden, waarschijnlijk veroorzaakt door verwoestende overstromingen
Een van Europa's ergste hongersnoden, waarschijnlijk veroorzaakt door verwoestende overstromingen Ongelukkige timing en snelheid van verandering kunnen voldoende zijn om een klimaatsysteem te kantelen
Ongelukkige timing en snelheid van verandering kunnen voldoende zijn om een klimaatsysteem te kantelen Kunnen kolenmijnen worden afgetapt voor zeldzame aardmetalen?
Kunnen kolenmijnen worden afgetapt voor zeldzame aardmetalen?  Onderzoek laat zien hoe gewone mensen ‘situationele helden’ kunnen worden
Onderzoek laat zien hoe gewone mensen ‘situationele helden’ kunnen worden
Hoofdlijnen
- Een doorbraak voor snelle, efficiënte productie van menselijke immuuncellen
- Begrijpt jouw hond het als je zegt ‘haal de bal’? Een nieuwe studie in Hongarije zegt van wel
- Wat is de naam van de studiebacteriën en -virussen?
- Waar zoeken de wetenschappers op bij het analyseren van gegevens?
- Wetenschappers begrijpen hoe de E. coli-kloon wereldwijd verspreid is geraakt
- Hoe leren ziekteverwekkers ziekteverwekkers te zijn:partnerschappen tussen microben die ziekten bij de mens leiden
- Wat bepaalt de sterkte van een arrheniusbasis?
- Hoe worden pulsars gevormd?
- Wat voor soort suiker is ribose?
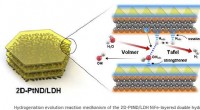
- Dubbellaagse katalysator genereert meer waterstof
- Elektrodepositie en gloeien gebruikt om de hardheid in nanokorrelige metalen aan te passen

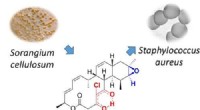
- Antimicrobieel natuurlijk product actief tegen zowel MRSA als malaria veroorzakende parasiet
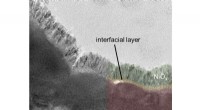
- Zonnewaterstof:fotoanodes beloven hoge efficiëntie
- Normaal een isolator, diamant wordt een metalen geleider wanneer het wordt blootgesteld aan grote spanning in een nieuw theoretisch model

 Next-gen membranen voor het afvangen van koolstof
Next-gen membranen voor het afvangen van koolstof Wat is de functie van celmambraan?
Wat is de functie van celmambraan?  Wanneer de snelheid van moleculen afneemt, neemt het drukgas ook af?
Wanneer de snelheid van moleculen afneemt, neemt het drukgas ook af?  Waarom moet een ruimtevaartuig een ontsnappingssnelheid bereiken om ruimte te kunnen hebben?
Waarom moet een ruimtevaartuig een ontsnappingssnelheid bereiken om ruimte te kunnen hebben?  Welk element is zeer kneedbaar en vrijwel niet-reactief?
Welk element is zeer kneedbaar en vrijwel niet-reactief?  Als kalksteen werd verpletterd, wat zou het dan doen met de reactiesnelheid tussen een zuur en kalksteen?
Als kalksteen werd verpletterd, wat zou het dan doen met de reactiesnelheid tussen een zuur en kalksteen?  Wetenschappers zien voor het eerst licht van achter een zwart gat
Wetenschappers zien voor het eerst licht van achter een zwart gat  Is bros een fysieke eigenschap van metaal?
Is bros een fysieke eigenschap van metaal?
- Elektronica
- Biologie
- Zonsverduistering
- Wiskunde
- French | Italian | Spanish | Portuguese | Swedish | German | Dutch | Danish | Norway |

-
Wetenschap © https://nl.scienceaq.com

