
Wetenschap
Wat moet een gas doorgaan, worden vast?
1. Condensatie: Het gas moet eerst afkoelen en energie verliezen. Dit zorgt ervoor dat de gasmoleculen vertragen en dichter bij elkaar komen. De aantrekkingskracht tussen de moleculen neemt toe en ze beginnen een vloeistof te vormen.
2. Bevriezen: Terwijl de vloeistof blijft afkoelen, vertragen de moleculen nog verder. Uiteindelijk worden ze vergrendeld in een vaste, rigide structuur en vormen ze een vaste stof.
Dit proces wordt depositie genoemd Wanneer het rechtstreeks van een gas naar een vaste stof voorkomt, slaat u het vloeibare stadium over.
Hier is een uitsplitsing van de veranderingen:
* gas: Moleculen liggen ver uit elkaar, bewegen snel en hebben zwakke attracties.
* vloeistof: Moleculen zijn dichter bij elkaar, bewegen langzamer en hebben sterkere attracties.
* solide: Moleculen zijn strak verpakt, trillen op zijn plaats en hebben zeer sterke attracties.
Voorbeelden:
* waterdamp (gas) -> water (vloeistof) -> ijs (vaste)
* koolstofdioxide (gas) -> droog ijs (vaste) (afzetting)
De exacte temperatuur en druk die nodig is voor deze veranderingen variëren afhankelijk van de specifieke stof.
 NASA observeert tropische storm Matmo in Noord-Centrale Golf van Bengalen
NASA observeert tropische storm Matmo in Noord-Centrale Golf van Bengalen De maan regelt het vrijkomen van methaan in de Noordelijke IJszee
De maan regelt het vrijkomen van methaan in de Noordelijke IJszee Een appel valt vanwege de zwaartekrachtattractie op de aarde. Hoe verhoudt de aarde zich?
Een appel valt vanwege de zwaartekrachtattractie op de aarde. Hoe verhoudt de aarde zich?  Wat is een voetpad? Een pad waarop mensen kunnen lopen?
Wat is een voetpad? Een pad waarop mensen kunnen lopen?  Welk dier leeft het langst?
Welk dier leeft het langst?
Hoofdlijnen
- Coyotes in New York City hoeven niet afhankelijk te zijn van menselijke voeding
- Onderzoek onthult hoe klimaatverandering de aquacultuur van Hawaiiaanse visvijvers kan beïnvloeden
- Wat zijn vijf manieren waarop organismen als fossiel kunnen worden bewaard?
- Waar wordt ATP het meest efficiënt geproduceerd?
- Wilde bijen worden bedreigd door huisbijen, invasieve soorten, ziekteverwekkers en klimaatverandering, maar wij kunnen helpen
- Hoe te voorkomen dat de nederige egel voor altijd uit de Britse tuinen en het platteland verdwijnt?
- Wat is de theorie achter genbanden?
- Wat reguleert maagmotiliteit en legen?
- Onderzoekers ontwikkelen een model om te laten zien hoe bacteriën groeien in sanitaire systemen
- Nieuwe krachtige analogen van plantenhormoon zorgen voor verlichting van droogtestress voor gewassen
- Door nieuwe technologie kunnen belangrijke metalen efficiënter worden gemaakt

- Een complete set van energieniveauposities van alle primaire metaalhalogenideperovskieten
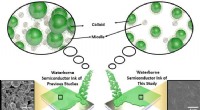
- Milieuvriendelijke halfgeleiderinkten op waterbasis met oppervlakteactieve stof
- Nieuwe legering om loodprobleem in drinkwater op te lossen

 Ringen maken Saturnus schaduwrijker, blauwer en minder wazig in de winter
Ringen maken Saturnus schaduwrijker, blauwer en minder wazig in de winter Wat is een actie die op een lichaam wordt uitgeoefend om de staat van rust of bewegingskracht te veranderen, heeft een grootte en richting?
Wat is een actie die op een lichaam wordt uitgeoefend om de staat van rust of bewegingskracht te veranderen, heeft een grootte en richting?  Hoeveel watt zal een ballast consumeren voor 3 20 tubelights?
Hoeveel watt zal een ballast consumeren voor 3 20 tubelights?  Mechanische hefboom berekenen
Mechanische hefboom berekenen Hoe de stroomsnelheid te berekenen met pijpmaat en druk
Hoe de stroomsnelheid te berekenen met pijpmaat en druk  De wereld heeft in 2017 veel meer zonne-energie dan fossiele energie-opwekkingscapaciteit toegevoegd
De wereld heeft in 2017 veel meer zonne-energie dan fossiele energie-opwekkingscapaciteit toegevoegd Hoe een model van de seizoenen van de aarde te maken
Hoe een model van de seizoenen van de aarde te maken Marvel-superhelden helpen ademen
Marvel-superhelden helpen ademen
- Elektronica
- Biologie
- Zonsverduistering
- Wiskunde
- French | Italian | Spanish | Portuguese | Swedish | German | Dutch | Danish | Norway |

-
Wetenschap © https://nl.scienceaq.com

