
Wetenschap
Is de aantrekkingskracht sterker in moleculen een vaste stof of vloeistof?
Dit is waarom:
* vaste stoffen: Deeltjes in vaste stoffen zijn strak gepakt en hebben een vaste, regelmatige opstelling. Deze nauwe nabijheid en orde leiden tot sterke intermoleculaire krachten (aantrekkingskrachten tussen moleculen) die de deeltjes stevig op hun plaats houden. Deze sterke krachten beperken de beweging, waardoor vaste stoffen hun rigide vorm en niet -samendrukbaarheid krijgen.
* vloeistoffen: Deeltjes in vloeistoffen zijn minder strak verpakt dan in vaste stoffen en hebben een minder geordende opstelling. De intermoleculaire krachten zijn zwakker in vloeistoffen, waardoor deeltjes vrijer kunnen bewegen en de vorm van hun container kunnen aannemen. Hoewel de krachten zwakker zijn dan in vaste stoffen, zijn ze nog steeds sterk genoeg om de deeltjes bij elkaar te houden, waardoor de vloeistof niet oneindig uitbreidt.
Samenvattend: De sterkte van intermoleculaire krachten bepaalt de toestand van materie. Vaste stoffen hebben sterke intermoleculaire krachten, vloeistoffen hebben zwakkere intermoleculaire krachten en gassen hebben zeer zwakke intermoleculaire krachten.
 Wetenschappers ontdekken breuksysteem in Zuidoost-Nepal
Wetenschappers ontdekken breuksysteem in Zuidoost-Nepal Zes vermisten na dodelijke Griekse overstromingen terwijl getroffen steden kampen met tekorten
Zes vermisten na dodelijke Griekse overstromingen terwijl getroffen steden kampen met tekorten Asbest in mulch op speelplaatsen:hoe voorkom je een herhaling van dit schandaal over de circulaire economie?
Asbest in mulch op speelplaatsen:hoe voorkom je een herhaling van dit schandaal over de circulaire economie?  Gebouwen verwarmen:de over het hoofd geziene klimaatveranderingsfactor
Gebouwen verwarmen:de over het hoofd geziene klimaatveranderingsfactor Welke laag in het regenwoud leeft Passion Flower Butterfly?
Welke laag in het regenwoud leeft Passion Flower Butterfly?
Hoofdlijnen
- Wat zit er in een naam? In sommige gevallen een langere levensduur
- Wereldprimeur gebruikt satellieten en oceaanmodellen om de biodiversiteit op de Antarctische zeebodem te verklaren
- Hoe verschilt de cel van een cellen organisme van cellen in veel gecellig organisme?
- Wat zijn de takken van de wetenschap die verband houden met de landbouw?
- Is een cel heterogeen of homogeen systeem?
- Wat wordt gebruikt om de genetische code van DNA -ribosomen te dragen?
- Hoe dierproeven werken
- Wat hebben de dochter- en oudercel gemeen?
- Wat is het substraat van maaglipase?
- Wetenschappers creëren aanpasbare, stofachtige stroombron voor draagbare elektronica

- Een theoretische studie verklaart de natuurlijke selectie van eiwitten
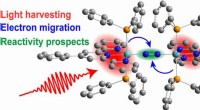
- Hoe zonlicht elektronen activeert om stikstof te breken en ammoniak te vormen
- De eiwitten die de biosynthese van formicamycine behouden

- Team ontwikkelt methode voor neurale netcomputing in water

 Pacific bereidt zich voor op Super Blood Moon hemelse show
Pacific bereidt zich voor op Super Blood Moon hemelse show Neerslag wordt steeds variabeler naarmate het klimaat warmer wordt
Neerslag wordt steeds variabeler naarmate het klimaat warmer wordt Nieuw mechanisme van radio-emissie in neutronensterren vrijgegeven
Nieuw mechanisme van radio-emissie in neutronensterren vrijgegeven Onderzoek zou de weg kunnen vrijmaken voor een beter begrip van de manier waarop planten en dieren groeien en zich ontwikkelen
Onderzoek zou de weg kunnen vrijmaken voor een beter begrip van de manier waarop planten en dieren groeien en zich ontwikkelen  Waarom citroen toegevoegd aan water is een omkeerbare verandering?
Waarom citroen toegevoegd aan water is een omkeerbare verandering?  Is melk een zuur of een alkali?
Is melk een zuur of een alkali?  Verschillende bronnen van water
Verschillende bronnen van water  Onderzoekers ontwikkelen een door licht aangedreven actuator met hoog koppel
Onderzoekers ontwikkelen een door licht aangedreven actuator met hoog koppel
- Elektronica
- Biologie
- Zonsverduistering
- Wiskunde
- French | Italian | Spanish | Portuguese | Swedish | German | Dutch | Danish | Norway |

-
Wetenschap © https://nl.scienceaq.com

