
Wetenschap
Hoe verschilt een vloeibaar water van vast ijs?
vloeibaar water:
* Moleculaire opstelling: Watermoleculen in vloeibare vorm zijn dicht bij elkaar, maar kunnen vrij bewegen. Ze hebben een ietwat willekeurige, constant verschuivende opstelling.
* Dichtheid: Water is dichter dan ijs. Dit is de reden waarom ijs zweeft.
* Vorm: Vloeibaar water krijgt de vorm van zijn container.
* Compressibiliteit: Vloeibaar water is relatief niet -samendrukbaar, wat betekent dat het volume veranderingen in het volume weerstaat wanneer de druk wordt uitgeoefend.
* Beweging: Watermoleculen in een vloeistof bewegen constant en botsen met elkaar. Deze beweging geeft water zijn vloeibaarheid.
vast ijs:
* Moleculaire opstelling: Watermoleculen in massief ijs zijn gerangschikt in een zeer geordende, kristallijne structuur. Ze zijn opgesloten in specifieke posities.
* Dichtheid: IJs is minder dicht dan vloeibaar water. Daarom zweeft het.
* Vorm: Vast ijs heeft een vaste vorm.
* Compressibiliteit: IJs is relatief onvergelijkbaar.
* Beweging: Watermoleculen in ijs zijn strak verpakt en trillen op zijn plaats, maar ze kunnen niet vrij bewegen.
Sleutelverschil: Het belangrijkste verschil tussen vloeibaar water en vast ijs is de mate van bewegingsvrijheid van de watermoleculen. In vloeibaar water hebben de moleculen meer vrijheid om te bewegen, terwijl ze in vast ijs worden vergrendeld in een vaste structuur.
Dit verschil in moleculaire opstelling verklaart waarom ijs drijft en waarom vloeibaar water kan stromen.
 Welke producten worden gemaakt wanneer koolwaterstoffen branden?
Welke producten worden gemaakt wanneer koolwaterstoffen branden?  Beschrijf twee veranderingen door de fusie van waterstof?
Beschrijf twee veranderingen door de fusie van waterstof?  Chemici zetten afval van plastic flessen om in sorptiemiddel voor insecten
Chemici zetten afval van plastic flessen om in sorptiemiddel voor insecten High-tech detectie verlicht stresstesten voor beton
High-tech detectie verlicht stresstesten voor beton Wat zie je als je kaliumchloride oplost met water?
Wat zie je als je kaliumchloride oplost met water?
 De helft van de wereldbevolking wordt blootgesteld aan toenemende luchtvervuiling, studie toont
De helft van de wereldbevolking wordt blootgesteld aan toenemende luchtvervuiling, studie toont Subtropische storm Andrea springt in het geweer als de eerste storm van het Atlantische seizoen van 2019
Subtropische storm Andrea springt in het geweer als de eerste storm van het Atlantische seizoen van 2019 Amerikaanse staat geeft belangrijke goedkeuring voor Keystone-pijplijn
Amerikaanse staat geeft belangrijke goedkeuring voor Keystone-pijplijn Mos dat arseen uit drinkwater kan verwijderen ontdekt
Mos dat arseen uit drinkwater kan verwijderen ontdekt De toekomst biedt uitdagingen en kansen voor zuivelproducenten
De toekomst biedt uitdagingen en kansen voor zuivelproducenten
Hoofdlijnen
- Waarom hebben cellen een klein oppervlak?
- Wat is 11Degease Celleneas in Fahrenheit?
- Vindt natuurlijke selectie plaats in tegenstelling tot evolutie?
- Van koralen tot gewassen:hoe het leven de plannen voor zijn cellulaire energiecentrales beschermt
- Waar bevindt het DNA zich in een cel?
- Diatomeeën slijmvormen en groene algen zijn wat?
- Kraaien kunnen bewust plannen hoeveel telefoontjes ze moeten plegen, zo blijkt uit studieprogramma's
- Wat hebben somatische cellen en gameten met elkaar gemeen?
- Een type passief transport over een celmembraan dat speciale dragers vereist is?
- Lithium-ionbatterijen krijgen meer efficiëntie dankzij silicium, germanium, koolstof nanowalls

- Onderzoekers verbeteren de synthese van bismutwolframaat met een milieuvriendelijke procedure
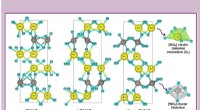
- De breuktaaiheid van het materiaal voor vliegtuigbouw wordt 1,5 keer verhoogd

- Staatsonderzoekers Sam Houston bestuderen DNA van explosieven

- Een sprong in het gebruik van silicium voor batterijanoden
 Wat beschrijft het beste de moderne definitie van een sterrenbeeld?
Wat beschrijft het beste de moderne definitie van een sterrenbeeld?  Met het BMI-systeem kunnen gebruikers de robotarm besturen terwijl hun handen bezig zijn met iets anders
Met het BMI-systeem kunnen gebruikers de robotarm besturen terwijl hun handen bezig zijn met iets anders Mars wacht
Mars wacht Wat is het belangrijkste onderdeel van de atmosfeer van Neptunes?
Wat is het belangrijkste onderdeel van de atmosfeer van Neptunes?  De magnetische polen van de aarde kunnen beginnen te kantelen. Wat gebeurt er dan?
De magnetische polen van de aarde kunnen beginnen te kantelen. Wat gebeurt er dan? Wat is het klimaat?
Wat is het klimaat?  3 luchtonderzoeken voltooid ter voorbereiding op Dark Energy Spectroscopic Instrument
3 luchtonderzoeken voltooid ter voorbereiding op Dark Energy Spectroscopic Instrument Wat is een categorie 5-storm?
Wat is een categorie 5-storm?
- Elektronica
- Biologie
- Zonsverduistering
- Wiskunde
- French | Italian | Spanish | Portuguese | Swedish | German | Dutch | Danish | Norway |

-
Wetenschap © https://nl.scienceaq.com

