
Wetenschap
Een molecuul met een positief en negatief gebied is?
Dit is waarom:
* polariteit: Polariteit in chemie verwijst naar de ongelijke verdeling van elektrische lading binnen een molecuul.
* elektronegativiteit: Deze ongelijke verdeling komt voort uit het verschil in elektronegativiteit tussen de atomen die het molecuul vormen. Elektronegativiteit is het vermogen van een atoom om elektronen naar zichzelf aan te trekken.
* Polaire bindingen: Wanneer twee atomen met aanzienlijk verschillende elektronegativiteiten binden, worden de elektronen dichter bij het meer elektronegatieve atoom getrokken, waardoor een gedeeltelijke negatieve lading op dat atoom en een gedeeltelijke positieve lading op het minder elektronegatieve atoom ontstaat. Dit creëert een polaire binding.
Voorbeelden van polaire moleculen:
* water (h₂o): Zuurstof is elektronegatiefer dan waterstof, waardoor de zuurstofzijde van het molecuul gedeeltelijk negatief is en de waterstofzijden gedeeltelijk positief.
* ammoniak (NH₃): Stikstof is elektronegatiefer dan waterstof, waardoor een gedeeltelijk negatief stikstofatoom en gedeeltelijk positieve waterstofatomen ontstaat.
* waterstofchloride (HCl): Chloor is elektronegatiefer dan waterstof, waardoor het chlooratoom een gedeeltelijke negatieve lading en het waterstofatoom een gedeeltelijke positieve lading krijgt.
Belangrijke opmerking: Niet alle moleculen met polaire bindingen zijn polaire moleculen. De algehele vorm van het molecuul beïnvloedt ook de polariteit. Als de polaire bindingen symmetrisch zijn gerangschikt, kunnen de kosten worden geannuleerd en is het molecuul niet -polair.
 Tin Vs. Loodgewicht
Tin Vs. Loodgewicht
Het gewicht van een element zoals tin of lood is een kwestie van zowel het atomaire gewicht - hoeveel een afzonderlijk atoom van het element weegt - als van zijn dichtheid. Hoe dichter de substantie, des te meer massa het per vo
 Hoeveel protonen zijn er in 1 mol No2 -gas?
Hoeveel protonen zijn er in 1 mol No2 -gas?  Doel van kalkwater met marmeren chip?
Doel van kalkwater met marmeren chip?  Ingenieurs ontwikkelen een plastic elektrode die uitrekt als rubber, maar elektriciteit transporteert als draden
Ingenieurs ontwikkelen een plastic elektrode die uitrekt als rubber, maar elektriciteit transporteert als draden Wat is reactiever barium of cesium?
Wat is reactiever barium of cesium?
Hoofdlijnen
- Onderzoeken waarom sprinkhanen vernietigende zwermen vormen
- Hoe maak je een celmodel van een Amoeba
- Welke structuren worden door prokaryoten gebruikt om aan oppervlakken te bevestigen?
- Waar is wetenschappelijk denken op gebaseerd?
- Ideeën voor Cookie Science Fair Projects
- Instrumenten gebruikt in de biologie
Biologen en biologiestudenten gebruiken verschillende instrumenten in hun werk om kennis over levende wezens te verzamelen. Deze instrumenten en hulpmiddelen worden elk jaar gedetailleerder en hightech, evenals
- Welk zoogdier heeft de meeste nefronen met een lange loop?
- Hoe gebruiken biologen wetenschappelijke notatie?
- Wat zegt een aanhoudende algenbloei over de gezondheidsplaneet?
- X-ray laser sight onthult medicijndoelen

- Onderzoekers onderzoeken de structuur van fosfaationische geleidende glazen met behulp van vastestof NMR
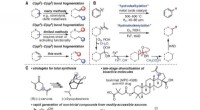
- Een efficiëntere manier om hangende olefinen te splitsen van terpenen en soortgelijke verbindingen
- Microscoop op een chip kan medische expertise naar verre patiënten brengen
- Het eerste hydrogelplatform in zijn soort maakt on-demand productie van medicijnen mogelijk, Chemicaliën

 Wat bedoel je met machtsbron?
Wat bedoel je met machtsbron?  Onderzoek toont mogelijke onbedoelde effecten van handvestschoolbewegingen aan
Onderzoek toont mogelijke onbedoelde effecten van handvestschoolbewegingen aan Vezeloptische detectiesonde:Quasi-3D plasmonische structuren op glasvezeluiteinden
Vezeloptische detectiesonde:Quasi-3D plasmonische structuren op glasvezeluiteinden Voedselzekerheid onder water vinden
Voedselzekerheid onder water vinden Wat is een voorbeeld van continentale continentale grens?
Wat is een voorbeeld van continentale continentale grens?  Wat is relativiteit?
Wat is relativiteit?  DNA-motor loopt langs nanobuis, transporteert kleine deeltjes
DNA-motor loopt langs nanobuis, transporteert kleine deeltjes Nederlands techbedrijf betrapt in rij VS-China
Nederlands techbedrijf betrapt in rij VS-China
- Elektronica
- Biologie
- Zonsverduistering
- Wiskunde
- French | Italian | Spanish | Portuguese | Swedish | German | Dutch | Danish | Norway |

-
Wetenschap © https://nl.scienceaq.com

