
Wetenschap
Wat maakt zwaveldioxide en water?
so₂ + h₂o ⇌ h₂so₃
Dit is wat er gebeurt:
* zwaveldioxide lost op in water: Dus₂ is een gas dat oplost in water.
* Vorming van zwavelzuur: Wanneer het oplost, reageert het met watermoleculen om zwavelzuur te vormen.
* evenwicht: De reactie is omkeerbaar, wat betekent dat het in beide richtingen kan doorgaan. Een deel van het zwavelzuur kan teruggaan tot zwaveldioxide en water.
Zwavelzuur is een zwak zuur, wat betekent dat het niet volledig in water ioniseert. Het kan echter bijdragen aan de zuurgraad van oplossingen, wat belangrijk is in processen zoals:
* zure regen: Zwaveldioxide vrijgegeven uit brandende fossiele brandstoffen lost in regenwater op om zwavelzuur te vormen, wat bijdraagt aan zure regen.
* Industriële processen: Zwavelzuur wordt gebruikt in sommige industriële processen, zoals de productie van papier en textiel.
Het is belangrijk op te merken dat zwaveldioxide ook kan reageren met andere stoffen in de atmosfeer, zoals zuurstof, om zwavelzuur (H₂so₄) te vormen, wat een sterker zuur is.
 Wat heb je waargenomen terwijl benzoëzuur-zoutzout smelt?
Wat heb je waargenomen terwijl benzoëzuur-zoutzout smelt?  Waarom is sterke nucleaire kracht alleen op korte afstanden?
Waarom is sterke nucleaire kracht alleen op korte afstanden?  Wetenschappers kunnen nu zuurstof in de structuur van katalysatoren lokaliseren met een precisie van een biljoenste meter
Wetenschappers kunnen nu zuurstof in de structuur van katalysatoren lokaliseren met een precisie van een biljoenste meter Wat is de formule voor bariumhydride?
Wat is de formule voor bariumhydride?  Wat zijn de liganden aanwezig in een anorganische complexe verbinding?
Wat zijn de liganden aanwezig in een anorganische complexe verbinding?
Hoofdlijnen
- Er is een gemakkelijke manier om mitose en meiose te begrijpen
- Waarom groeit algen snel met kunstmest?
- Wat gebeurt er met de bacteriën als het wordt gemengd met witte bloedcellen?
- Welk organisme wordt gebruikt om gisting te bestuderen?
- Waarom is de celgrootte belangrijk?
- Wat zijn restrictie -enzymen?
- Welke buitenste bedekking van de dierencel?
- Hoe verschilt DNA & RNA?
- Hoe drie hardnekkige riffen kunnen helpen de mondiale oesterpopulaties te herstellen
- Middeleeuwse kruitrecepten opblazen

- Speeksel kan smaakvoorkeuren beïnvloeden

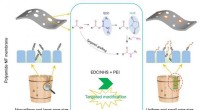
- Nieuwe gerichte modificatiestrategie verbetert de selectiviteit van polyamide nanofiltratiemembranen
- Elektrochemische cel haalt lithium uit zeewater

- Nieuwe experimentele inzichten stellen onderzoekers in staat eiwit-DNA-interacties met grotere precisie te onderzoeken
 Hoe is elektrische energie vergelijkbaar met mechanische en geluidsenergie?
Hoe is elektrische energie vergelijkbaar met mechanische en geluidsenergie?  Wat is de frequentie van warmtestraling?
Wat is de frequentie van warmtestraling?  Consumentenonderzoeken stuwen aandelenkoersen op, uit onderzoek blijkt
Consumentenonderzoeken stuwen aandelenkoersen op, uit onderzoek blijkt Hoe Spaanse en Aziatische bevolkingsgroepen de Amerikaanse eetcultuur beïnvloeden
Hoe Spaanse en Aziatische bevolkingsgroepen de Amerikaanse eetcultuur beïnvloeden Kunnen mensen superkrachten hebben?
Kunnen mensen superkrachten hebben?  Waarom wordt waterstof verzameld door neerwaartse verplaatsing van water?
Waarom wordt waterstof verzameld door neerwaartse verplaatsing van water?  Welke energiebron gebruikt een gloeilamp?
Welke energiebron gebruikt een gloeilamp?  Welke term beschrijft bacteriën die rond of sferisch gevormd zijn?
Welke term beschrijft bacteriën die rond of sferisch gevormd zijn?
- Elektronica
- Biologie
- Zonsverduistering
- Wiskunde
- French | Italian | Spanish | Portuguese | Swedish | German | Dutch | Danish | Norway |

-
Wetenschap © https://nl.scienceaq.com

