
Wetenschap
Waarom is AG CL oplosbaar in natriumthiosulfaat?
* Agcl is een spaarzaam oplosbaar zout. Het heeft een zeer lage oplosbaarheidsproductconstante (KSP), wat betekent dat het niet gemakkelijk oplost in water.
* Thiosulfate-ionen (S2O3^2-) zijn goede liganden. Ze kunnen coördinaatbindingen vormen met zilverionen (Ag+).
* Complex ionenvorming: Wanneer AGCL wordt toegevoegd aan een natriumthiosulfaatoplossing, treedt de volgende reactie op:
Agcl (s) + 2S2O3^2- (aq) ⇌ [Ag (S2O3) 2]^3- (aq) + cl- (aq)
Deze reactie resulteert in de vorming van een stabiele complexion, [Ag (S2O3) 2]^3- , de dicyanoargentate (i) ion genoemd . Deze complexe ion is oplosbaar in water, waardoor zilverionen effectief uit oplossing worden verwijderd en het evenwicht naar rechts drijven, waardoor meer AgCl oplost.
Samenvattend:
De oplosbaarheid van AGCL in natriumthiosulfaat is niet te wijten aan direct oplossen van AGCL in de thiosulfaatoplossing. In plaats daarvan wordt het aangedreven door de vorming van een oplosbaar complexion, [Ag (S2O3) 2]^3-, die zilverionen uit oplossing verwijdert, waardoor meer agcl kan oplossen. Dit proces staat bekend als complexering .
Hoofdlijnen
- Waarom is stikstof belangrijk voor planten?
- Welke structuur in het urinestelsel is het belangrijkst?
- Wat is het pad van een zuurstofmolecuul wanneer het het menselijk lichaam binnenkomt?
- Wat zijn tests voor eiwitten?
- Een vlieg heeft twee allelen voor de kleur van zijn ogen. Het groene allel is recessief en wordt vertegenwoordigd door blauw dominant, p. Als er 28 organismen zijn, welke p?
- Nieuwe CRISPR-tool richt zich op RNA in zoogdiercellen
- Wat is de tak van de wetenschap die groepen cellen bestudeert en hoe ze samenwerken?
- Welke onderlinge relaties heeft het endocriene systeem met andere orgaansystemen?
- Zijn er subsystemen binnen het spijsverteringssysteem?
- Video:Waarom exploderen telefoonbatterijen soms?

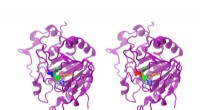
- Simulatie van het AsqJ-enzym opent nieuwe mogelijkheden voor farmaceutische chemie
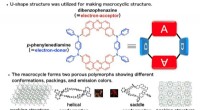
- Unieke organische lichtemitterende moleculaire emitters
- Borstimplantaten markeren met tomaten-DNA om namaak te voorkomen

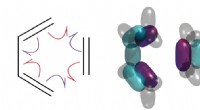
- Theoretici bewijzen eindelijk dat gekrulde pijlen de waarheid vertellen over chemische reacties
 Welk metaal bestaat uit de ertsenzink en lood?
Welk metaal bestaat uit de ertsenzink en lood?  Nieuw rapport beveelt een landelijke inspanning aan om de methaanemissies beter in te schatten
Nieuw rapport beveelt een landelijke inspanning aan om de methaanemissies beter in te schatten Oudste Scandinavisch menselijk DNA gevonden in oude kauwgom
Oudste Scandinavisch menselijk DNA gevonden in oude kauwgom Wat is 10 graden noord en 39 oost?
Wat is 10 graden noord en 39 oost?  De waarde van zeegras bij het veiligstellen van een duurzame planeet
De waarde van zeegras bij het veiligstellen van een duurzame planeet Cassini op weg naar de laatste ontmoeting met Titan
Cassini op weg naar de laatste ontmoeting met Titan Frankrijk nadert telefoonverbod op scholen vanaf september
Frankrijk nadert telefoonverbod op scholen vanaf september Hoe amplitude werkt?
Hoe amplitude werkt?
- Elektronica
- Biologie
- Zonsverduistering
- Wiskunde
- French | Italian | Spanish | Portuguese | Swedish | German | Dutch | Danish | Norway |

-
Wetenschap © https://nl.scienceaq.com


