
Wetenschap
Wat is het verschil tussen lithium 6 en lithum 7 op periodieke tabel?
Hier is de uitsplitsing:
* lithium-6: Heeft 3 protonen en 3 neutronen . De atoommassa is ongeveer 6.
* lithium-7: Heeft 3 protonen en 4 neutronen . De atoommassa is ongeveer 7.
Belangrijkste verschillen:
* massa: Lithium-7 is zwaarder dan lithium-6 vanwege het extra neutron.
* Natuurlijke overvloed: Lithium-7 is veel overvloediger van aard (92,5%) dan lithium-6 (7,5%).
* Nucleaire eigenschappen: Lithium-6 wordt gebruikt in nucleaire fusiereacties, terwijl lithium-7 wordt gebruikt bij medische beeldvorming en therapie.
Periodieke tabel:
De periodieke tabel vermeldt alleen de gemiddelde atoommassa van lithium, dat is ongeveer 6.941. Dit gemiddelde weerspiegelt de relatieve overvloed van de twee isotopen.
Samenvattend:
Het verschil tussen lithium-6 en lithium-7 ligt in hun neutronentelling, dat hun massa en sommige van hun nucleaire eigenschappen beïnvloedt. Hoewel het periodiek systeem zich niet onderscheidt tussen isotopen, is het belangrijk om te begrijpen dat elementen kunnen bestaan in verschillende isotopische vormen.
 Zonne- en windenergie behouden grondwater voor droogte, landbouw
Zonne- en windenergie behouden grondwater voor droogte, landbouw Wat is het verschil tussen een levende en niet -ding?
Wat is het verschil tussen een levende en niet -ding?  Projecties voor zeespiegelstijging vertroebeld door antarctische instabiliteit
Projecties voor zeespiegelstijging vertroebeld door antarctische instabiliteit NASA telt de regen van Albertos op in het zuidoosten van de VS en Tennessee Valley
NASA telt de regen van Albertos op in het zuidoosten van de VS en Tennessee Valley Amerikaanse houtindustrie verlamd door dubbele klap van handelsoorlog en COVID-19
Amerikaanse houtindustrie verlamd door dubbele klap van handelsoorlog en COVID-19
Hoofdlijnen
- Cellulaire ademhaling in planten
- Wat betekenen de gegevens in een wetenschappelijk project?
- Wanneer komt het vetkatabolisme meestal voor?
- Wat is het ‘oudste dochtersyndroom’ en hoe kunnen we dit verhelpen?
- Waarom eet je in een lab?
- Wat definieer reproductie?
- Wat is een interne regulator van de celcyclus?
- Wat zijn de special in celmembraan waarmee materialen zoals water en suiker door maakten worden doorgemaakt?
- Wat doen planten met extra glucose?
- Wetenschappers kweken snel een DKDP-kristal met lange zaden

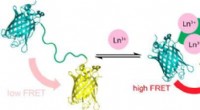
- Nieuwe sensor detecteert zeldzame metalen die in smartphones worden gebruikt
- Nieuwe antimicrobiële coating kan de sleutel zijn in de strijd tegen ziekenhuisinfecties

- Wetenschappers ontwikkelen nieuwe chip voor snelle en nauwkeurige ziektedetectie tegen lage kosten

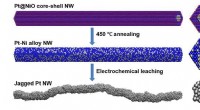
- Ruwe oppervlakken bieden extra locaties voor energieopwekkende reacties in brandstofcellen
 Welke middelen brengen chemische verwering op rotsen te bewerkstelligen A.RAINWATER B.OCEAN WATER C. FLANDEN D. allemaal?
Welke middelen brengen chemische verwering op rotsen te bewerkstelligen A.RAINWATER B.OCEAN WATER C. FLANDEN D. allemaal?  De effecten van chloor op de watergeleidbaarheid
De effecten van chloor op de watergeleidbaarheid Uitgebreid overzicht van de belangrijke rollen en regulerende mechanismen van lncRNA's in groenten en fruit
Uitgebreid overzicht van de belangrijke rollen en regulerende mechanismen van lncRNA's in groenten en fruit  Het Panamakanaal voorkomt voorlopig een crisis, maar ten koste van het drinkwater
Het Panamakanaal voorkomt voorlopig een crisis, maar ten koste van het drinkwater  Waarom is waterstof H plus?
Waarom is waterstof H plus?  Wat voor soort suiker is geen glucose?
Wat voor soort suiker is geen glucose?  Vier basiseenheden in het metrieke stelsel die op het punt staan te worden gewijzigd
Vier basiseenheden in het metrieke stelsel die op het punt staan te worden gewijzigd Een nieuwe vorm van ijzer voor de verrijking van voedingsmiddelen
Een nieuwe vorm van ijzer voor de verrijking van voedingsmiddelen
- Elektronica
- Biologie
- Zonsverduistering
- Wiskunde
- French | Italian | Spanish | Portuguese | Swedish | German | Dutch | Danish | Norway |

-
Wetenschap © https://nl.scienceaq.com

