
Wetenschap
Is waterstofargon natriumstikstofzuurstof of clorine het minst waarschijnlijk om met andere elementen te reageren?
* Nobele gassen: Argon is een edel gas. Nobele gassen hebben een volledige buitenste schaal van elektronen, waardoor ze ongelooflijk stabiel en niet -reactief zijn. Ze winnen of verliezen niet gemakkelijk elektronen om bindingen te vormen.
Laten we eens kijken naar de andere elementen:
* waterstof (h): Waterstof is zeer reactief en vormt vaak bindingen met andere elementen.
* natrium (NA): Natrium is een zeer reactief metaal dat gemakkelijk een elektron verliest om positieve ionen te vormen.
* stikstof (n): Stikstof is relatief niet -reactief bij kamertemperatuur, maar kan onder bepaalde omstandigheden sterke bindingen vormen.
* zuurstof (O): Zuurstof is een zeer reactief element, essentieel voor verbranding en vele andere reacties.
* chloor (CL): Chloor is een zeer reactief niet -metaal dat elektronen gemakkelijk krijgt om negatieve ionen te vormen.
Samenvattend: De stabiele elektronenconfiguratie van Argon maakt het de minst waarschijnlijk om met andere elementen te reageren.
 Is crème een compound of mengsel?
Is crème een compound of mengsel?  Wat is het product van C14H30 dat wordt verbrand als brandstof en zinkmetaal dat in een oplossing van koper-2-nitraat terechtkomt?
Wat is het product van C14H30 dat wordt verbrand als brandstof en zinkmetaal dat in een oplossing van koper-2-nitraat terechtkomt?  Onderzoek identificeert een chemisch mechanisme dat laat zien hoe ijzer in de bodem arseen kan immobiliseren
Onderzoek identificeert een chemisch mechanisme dat laat zien hoe ijzer in de bodem arseen kan immobiliseren  Polymeermembranen kunnen baat hebben bij een duik
Polymeermembranen kunnen baat hebben bij een duik Is natriumaluminiumfosfaat een ionische verbinding?
Is natriumaluminiumfosfaat een ionische verbinding?
 Welke aanpassingen hebben vissen?
Welke aanpassingen hebben vissen?  Ambtenaren:Meer dan 40 procent van Californië uit droogte
Ambtenaren:Meer dan 40 procent van Californië uit droogte Studie onthult dreiging van catastrofale supervulkaanuitbarstingen die altijd aanwezig zijn
Studie onthult dreiging van catastrofale supervulkaanuitbarstingen die altijd aanwezig zijn Het vervangen van bomen door bamboe halveert de koolstofopslagcapaciteit van bossen
Het vervangen van bomen door bamboe halveert de koolstofopslagcapaciteit van bossen Leven de grootste dieren in de bosbodem van een tropisch regenwoud?
Leven de grootste dieren in de bosbodem van een tropisch regenwoud?
Hoofdlijnen
- Drang om samen te voegen:begrijpen hoe cellen samensmelten
- Waar kunnen leraren gratis kruiswoordpuzzels krijgen over microbiologie?
- Welke organismen met DNA als hun genetische moleculen het enzymenpolymerase?
- Wat zijn de dieren die bio -magnetisme gebruiken?
- Wat moet Finny Train Gene doen?
- Ontdekking van transcriptiefactor-eiwit dat koudetolerantie in rijst reguleert
- Waarom produceren enkele planten zaden die met succes onder water ontkiemen?
- Hebben molluskcellen een kern?
- Wanneer DNA wordt gerepliceerd, dient het oorspronkelijke molecuul als een (n)?
- Nieuw raamwerk past machine learning toe op atomistische modellering

- Eiwitvoeding voor cellen en organismen:kunnen we het gebruiken om ziekten te behandelen?
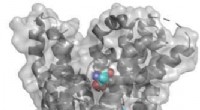
- Onderzoek onthulde de allereerste kristalstructuur van de dopamine 2-receptor gebonden aan een antipsychoticum

- Doorbraak in het benutten van de kracht van biologische katalysatoren

- De ontwikkeling van laagdimensionale nanomaterialen kan een revolutie teweegbrengen in toekomstige technologieën
 Mollen berekenen in een reactie
Mollen berekenen in een reactie Hoe moleculaire voetballen barsten in een röntgenlaserstraal
Hoe moleculaire voetballen barsten in een röntgenlaserstraal Hoe verandert de hoeveelheid daglicht en positie in de lucht met elk seizoen?
Hoe verandert de hoeveelheid daglicht en positie in de lucht met elk seizoen?  Wat zijn de twee belangrijkste delen van de wetenschap?
Wat zijn de twee belangrijkste delen van de wetenschap?  Hoe een deeltje stil kan staan in roterende ruimtetijd
Hoe een deeltje stil kan staan in roterende ruimtetijd  Is een ecosysteem of herbivoren voedingsstoffen en mineralen het belangrijkst in de voedselketen?
Is een ecosysteem of herbivoren voedingsstoffen en mineralen het belangrijkst in de voedselketen?  Waarom heette het sterrenbeeld Leo Leo?
Waarom heette het sterrenbeeld Leo Leo?  Wanneer voorwaardelijke vrijlating, reclasseringswerkers kiezen voor empathie, keert terug naar de gevangenis
Wanneer voorwaardelijke vrijlating, reclasseringswerkers kiezen voor empathie, keert terug naar de gevangenis
- Elektronica
- Biologie
- Zonsverduistering
- Wiskunde
- French | Italian | Spanish | Portuguese | Swedish | German | Dutch | Danish | Norway |

-
Wetenschap © https://nl.scienceaq.com

