
Wetenschap
Is stikstofwaterstof een ionische of covalente binding?
Stikstof en waterstof vormen een covalente binding . Dit is waarom:
* elektronegativiteit: Stikstof (N) heeft een elektronegativiteit van 3,0, terwijl waterstof (H) een elektronegativiteit van 2.1 heeft. Het verschil in elektronegativiteit is niet groot genoeg om een volledige overdracht van elektronen te creëren, die kenmerkend is voor ionische bindingen.
* delen van elektronen: In plaats van elektronen over te dragen, delen stikstof en waterstof elektronen om een stabiele octetconfiguratie te bereiken. Dit delen van elektronen vormt een covalente binding.
Daarom is de verbinding gevormd door stikstof en waterstof, ammoniak (NH3), een covalente verbinding.
 Naarmate de temperatuur stijgt, De aarde ademt zwaarder
Naarmate de temperatuur stijgt, De aarde ademt zwaarder Kritisch denken gebruiken om valse klimaatclaims te herkennen
Kritisch denken gebruiken om valse klimaatclaims te herkennen Chesapeake Bay:groter dan gemiddelde zomervoorspelling voor 2018 na natte lente
Chesapeake Bay:groter dan gemiddelde zomervoorspelling voor 2018 na natte lente Is Spanish Moss Giftig?
Is Spanish Moss Giftig?  Welke rol hebben regen en wind bij het veranderen van een soort rots in een andere rots?
Welke rol hebben regen en wind bij het veranderen van een soort rots in een andere rots?
Hoofdlijnen
- Wat is een kenmerk dat levende dingen helpt om te overleven en zich voort te planten?
- Hoe reageren op een veranderende omgeving gepaard gaat met het remmen van eerder gedrag
- Welke organismen produceren cellulose?
- Hoe voorkomt uitdroging dat microben groeien in voedsel?
- Café, croissant, wormen? EU-agentschap zegt dat wormen veilig zijn om te eten
- Onderzoekers tonen aan dat dieren zich kunnen aanpassen aan steeds vaker voorkomende koudemomenten
- Bevat een voedselweb slechts één roofdier en ketting?
- Wat is suiker in DNA?
- Waarom worden benige vissen als omnivoren beschouwd in de visserijsport?
- Bindmiddelvrij titanosilicaat van het type MWW voor selectieve en duurzame epoxidatie van propyleen
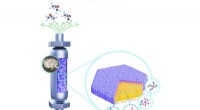
- Zwarte fosfor belooft de toekomst van elektronica

- Verhoogde bruikbaarheid en precisie bij vasculaire beeldvorming
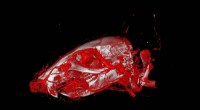
- Het degradatiegedrag van geavanceerde medische apparaten voorspellen

- Wetenschappers ontwikkelen nieuwe technologie voor de winning van non-ferro en edelmetalen

 Vlinders, bijen, insecten en meer:de zomer van het tellen van insecten begint in Duitsland
Vlinders, bijen, insecten en meer:de zomer van het tellen van insecten begint in Duitsland  Stanford Doggo:een zeer wendbare viervoeter
Stanford Doggo:een zeer wendbare viervoeter Wat zijn enkele mythen van Apollo?
Wat zijn enkele mythen van Apollo?  Afbeelding:James Webb Space Telescope-spiegel in volle bloei gezien
Afbeelding:James Webb Space Telescope-spiegel in volle bloei gezien Wat probeerden de romantici na te denken over de natuurlijke wereld?
Wat probeerden de romantici na te denken over de natuurlijke wereld?  Gaan moleculen bij absolute nul verdwijnen?
Gaan moleculen bij absolute nul verdwijnen?  Waar slaan lipiden energie op?
Waar slaan lipiden energie op?  Wat is de mechanische energie van een voetbal tijdens de pas?
Wat is de mechanische energie van een voetbal tijdens de pas?
- Elektronica
- Biologie
- Zonsverduistering
- Wiskunde
- French | Italian | Spanish | Portuguese | Swedish | German | Dutch | Danish | Norway |

-
Wetenschap © https://nl.scienceaq.com

