
Wetenschap
Element X bestaat als een niet-polair molecuul gemaakt van twee identieke atomen wanneer individueel element reageert met natrium ze vormen ionen 2- lading Welke groep behoort?
* Niet -polair molecuul met twee identieke atomen: Dit suggereert een diatomee molecuul, zoals H₂ (waterstof), N₂ (stikstof), O₂ (zuurstof), F₂ (fluor), Cl₂ (chloor), Br₂ (bromine) of I₂ (jodium).
* vormt ionen met een 2- lading bij het reageren met natrium: Dit betekent dat element X twee elektronen wint om een stabiele octetconfiguratie te bereiken.
het bepalen van de groep:
Elementen die twee elektronen krijgen om een stabiel octet te bereiken, worden gevonden in groep 16 (via) van het periodiek systeem. Deze groep staat ook bekend als de chalcogens .
Voorbeeld:
Zuurstof (O) is een goed voorbeeld. Het vormt een diatomee molecuul (O₂) en reageert met natrium om natriumoxide (Na₂o) te vormen, waarbij zuurstof een 2-lading heeft.
Daarom behoort element X tot groep 16 (via) van de periodiek systeem.
 Onderzoekers synthetiseren antimalariamoleculen gevonden in een schimmel uit Nunavut
Onderzoekers synthetiseren antimalariamoleculen gevonden in een schimmel uit Nunavut Als je zoveel opgeloste opgeloste stof toevoegt dat niet meer oplost, wat heeft dan?
Als je zoveel opgeloste opgeloste stof toevoegt dat niet meer oplost, wat heeft dan?  Naast gassen bevat de atmosfeer vele soorten kleine vaste stoffen?
Naast gassen bevat de atmosfeer vele soorten kleine vaste stoffen?  Wat zijn de smeltende en kookpunten van astatine?
Wat zijn de smeltende en kookpunten van astatine?  Chemici produceren uit één uitgangsmateriaal alle acht mogelijke varianten van polypropionaatbouwstenen
Chemici produceren uit één uitgangsmateriaal alle acht mogelijke varianten van polypropionaatbouwstenen
 Een door droogte geteisterde stad in Californië zinkt in de grond
Een door droogte geteisterde stad in Californië zinkt in de grond Is de aarde meestal land of water?
Is de aarde meestal land of water?  Tyfoon Phanfone verpest Kerstmis voor duizenden Filippino's
Tyfoon Phanfone verpest Kerstmis voor duizenden Filippino's Onderzoekers maken wereldwijde arseen-in-grondwaterkaarten om bedreigingen te markeren
Onderzoekers maken wereldwijde arseen-in-grondwaterkaarten om bedreigingen te markeren Perm-vulkanisme heeft bijgedragen aan het broeikasgasgehalte in de atmosfeer op Antarctica
Perm-vulkanisme heeft bijgedragen aan het broeikasgasgehalte in de atmosfeer op Antarctica
Hoofdlijnen
- Wie waren de mannen die betrokken waren bij de celtheorie?
- Wat geeft het aantal exemplaren basischromosomen aan?
- Moderne genetische sequencing-instrumenten geven een duidelijker beeld van hoe koralen verwant zijn
- Hoe stijgen en zinken vissen in het water?
- Wat maken alle biotische en abotische factoren in een bepaald gebied uit?
- Worden aminozuren slechts door één codon weergegeven?
- Wat is een auditieve bereik in de wetenschap?
- Hoe werkt het skelet- en gespierde systeem in een spin?
- Een factor die soorten gescheiden houdt, is?
- de tijdloze, complementaire smaak van oesters en champagne - uitgelegd

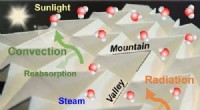
- Origami inspireert zeer efficiënte zonne-stoomgenerator
- Het plastictekort oplossen met een nieuwe chemische katalysator
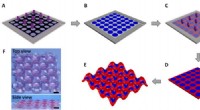
- Hydrogels met periodiek patroon:een model voor coöperatieve vervorming
- Ongrijpbare verbindingen van broeikasgas geïsoleerd

 Een kleine duw voor een robot,
Een kleine duw voor een robot,  Sommigen zeggen dat we bosbranden eerder hebben gezien dan dit, maar ze negeren de belangrijkste feiten
Sommigen zeggen dat we bosbranden eerder hebben gezien dan dit, maar ze negeren de belangrijkste feiten Wat betekent de stelling van de werk-kinetische energie in woorden?
Wat betekent de stelling van de werk-kinetische energie in woorden?  's Werelds eerste diamanten nano-elektromechanische schakelaar
's Werelds eerste diamanten nano-elektromechanische schakelaar Heeft er ooit een uitlijning o alle planeten van uw zonnestelsel?
Heeft er ooit een uitlijning o alle planeten van uw zonnestelsel?  Onderzoekers vinden valluik in SwissVote-verkiezingssysteem
Onderzoekers vinden valluik in SwissVote-verkiezingssysteem Welke metalen wenden zich tot gassen bij kamertemperatuur?
Welke metalen wenden zich tot gassen bij kamertemperatuur?  Kun jij een betere stoel bouwen?
Kun jij een betere stoel bouwen?
- Elektronica
- Biologie
- Zonsverduistering
- Wiskunde
- French | Italian | Spanish | Portuguese | Swedish | German | Dutch | Danish | Norway |

-
Wetenschap © https://nl.scienceaq.com

