
Wetenschap
Hoeveel koolstofatomen zijn er nodig om 12.011 gram te evenaren?
Het duurt 6.022 x 10^23 Koolstofatomen gelijk aan 12.011 gram.
Dit is waarom:
* Atomische massa: De atoommassa van koolstof is 12.011 atomaire massa -eenheden (AMU). Dit betekent dat één koolstofatoom 12.011 AMU weegt.
* mol: Een mol is een meeteenheid die een specifiek aantal deeltjes vertegenwoordigt (atomen, moleculen, enz.). Eén mol van elke stof bevat 6,022 x 10^23 deeltjes (het nummer van Avogadro).
* gram: De atomaire massa van een element in AMU is numeriek gelijk aan de massa van één mol van dat element in gram. Dus weegt een mol koolstof 12.011 gram.
Aangezien één mol koolstof 6.022 x 10^23 atomen bevat en 12.011 gram weegt, is er veel koolstofatomen nodig om 12,011 gram te evenaren.
 Hoe u klimaatverandering kunt voorspellen vanuit uw luie stoel
Hoe u klimaatverandering kunt voorspellen vanuit uw luie stoel Kokosverwarring onthult consumentenraadsel
Kokosverwarring onthult consumentenraadsel Landbouwintensivering geen blauwdruk voor duurzame ontwikkeling
Landbouwintensivering geen blauwdruk voor duurzame ontwikkeling Nieuwe modellen voorspellen minder door bliksem veroorzaakte ontstekingen, maar grotere bosbranden tegen het midden van de eeuw
Nieuwe modellen voorspellen minder door bliksem veroorzaakte ontstekingen, maar grotere bosbranden tegen het midden van de eeuw Interessante feiten over leeuwen en dieren
Interessante feiten over leeuwen en dieren
Hoofdlijnen
- Wat is de koolhydraten in plantencelwanden?
- Wolf huilen? Debat over de aanwezigheid van wolven in het noordoosten
- Welke rol speelt cytokinese tijdens de celcyclus?
- Wat is het herschikking van Gene?
- Hoe wordt ATP gebruikt?
- Welke wetenschapper die verantwoordelijk is voor het weerleggen van de theorie van spontane generatie?
- In de strijd tegen virale infectie, spelling telt
- Een nieuwe bevinding over hoe het chikungunya-virus zich heeft verspreid naar nieuwe vectoren en locaties
- Hoe liet experiment zien dat de bacteriën niet in bouillon ontstaan?
- Eenvoudige methode voor op keramiek gebaseerde flexibele elektrolytplaten voor lithium-metaalbatterijen

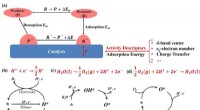
- Activiteitsbeschrijvingen voor elektrokatalysatoren in toepassingen voor energieopslag
- Een vreemd fenomeen ontrafelen dat zowel de prestaties van lithium-ionbatterijen helpt als schaadt

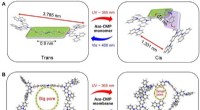
- Microporeuze polymeermembranen voor licht-gated ionentransport
- Nieuwe synthesemethode levert afbreekbare polymeren op

 Welk synthetisch polymeer wordt moeilijker naarmate het aantal koolstofatomen in de keten toeneemt?
Welk synthetisch polymeer wordt moeilijker naarmate het aantal koolstofatomen in de keten toeneemt?  Hoe schoolsluitingen voor COVID-19 de ongelijkheid vergroten
Hoe schoolsluitingen voor COVID-19 de ongelijkheid vergroten Het blootleggen van de tarotkaart voor matigheid
Het blootleggen van de tarotkaart voor matigheid  Hoe verschilt de grond van plaats tot plaats?
Hoe verschilt de grond van plaats tot plaats?  In welk jaar veranderde een aardbeving de loop van de Mississippi -rivier?
In welk jaar veranderde een aardbeving de loop van de Mississippi -rivier?  Noodtoestand uitgeroepen voor door bosbranden bedreigd Canberra
Noodtoestand uitgeroepen voor door bosbranden bedreigd Canberra Waarom zijn de fossielen onderaan ouder dan bovenaan de grond?
Waarom zijn de fossielen onderaan ouder dan bovenaan de grond?  Bewijs van twee aardbevingen verlengt breukgeschiedenis in Grand Tetons National Park
Bewijs van twee aardbevingen verlengt breukgeschiedenis in Grand Tetons National Park
- Elektronica
- Biologie
- Zonsverduistering
- Wiskunde
- French | Italian | Spanish | Portuguese | Swedish | German | Dutch | Danish | Norway |

-
Wetenschap © https://nl.scienceaq.com

