
Wetenschap
Het chloride -ion heeft dezelfde valentie als natrium, maar het is een andere elektrovalcency waarom?
valentie
* Valentie verwijst naar de combinatiecapaciteit van een atoom of ion. Het is een algemene term die beschrijft hoeveel bindingen een atoom kan vormen.
* Zowel natrium (NA) als chloor (CL) hebben een valentie van 1. Dit betekent dat ze de ene enkele binding met een ander atoom kunnen vormen.
elektrovency
* Elektroventie is het aantal elektronen dat een atoom wint of verliest om een ion te vormen. Het is specifiek voor ionische binding.
* Natrium (NA) heeft een elektroventie van +1 omdat het één elektron verliest om een positief geladen ion te worden (Na +).
* Chloor (CL) heeft een elektroventie van -1 omdat het één elektron krijgt om een negatief geladen ion te worden (Cl-).
Waarom het verschil?
Het verschil in elektravalentie komt voort uit de verschillende manieren waarop natrium en chloor een stabiele elektronenconfiguratie bereiken:
* natrium: Natrium heeft één elektron in zijn buitenste schaal. Door dit elektron te verliezen, bereikt het een stabiele configuratie met een volledige buitenste schaal (zoals de Noble Gas Neon).
* chloor: Chloor heeft zeven elektronen in zijn buitenste schaal. Door één elektron te krijgen, bereikt het ook een stabiele configuratie met een volledige buitenste schaal (zoals de edelgas argon).
Samenvattend:
* Zowel natrium als chloor hebben een valentie van 1, wat betekent dat ze één binding kunnen vormen.
* Natrium verliest een elektron om Na + te worden (elektrovalentie +1).
* Chloor krijgt een elektron om Cl- te worden (elektrovalentie -1).
Laat het me weten als je nog andere vragen hebt!
 Geo-engineering versus een vulkaan
Geo-engineering versus een vulkaan Hoe luchtvervuiling veranderde tijdens COVID-19 in Park City, Utah
Hoe luchtvervuiling veranderde tijdens COVID-19 in Park City, Utah Nieuw onderzoek identificeert patronen van boomdistributie in Afrikaanse savannes
Nieuw onderzoek identificeert patronen van boomdistributie in Afrikaanse savannes Groenten irrigeren met afvalwater in Afrikaanse steden kan ziektes verspreiden
Groenten irrigeren met afvalwater in Afrikaanse steden kan ziektes verspreiden De kust in het noordoosten van de VS is een hotspot voor het broeikaseffect
De kust in het noordoosten van de VS is een hotspot voor het broeikaseffect
Hoofdlijnen
- Veel dierenartsen praten niet graag over dikke katten
- Hoe bedenken wetenschappers met vragen?
- Mediterrane wijnmakerijen bevinden zich in een klimaathotspot. Klimatologen helpen hen zich aan te passen
- Wetenschappers ontdekken hoe weefselspanning de celdeling regelt
- Welk deel van de dierlijke cel geeft vorm aan de cel?
- Hoe nieuwe vogelsoorten ontstaan
- Wat reguleert de eiwitproductie in de kern?
- Geef de haaien niet de schuld:uit onderzoek blijkt waarom er steeds meer gehaakte tarpoenen worden gegeten
- Klimaatverandering zorgt ervoor dat boompopulaties wegblijven van de bodemschimmels die hen in stand houden
- Algoritmen en lasers temmen chemische reactiviteit

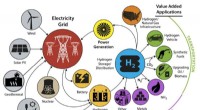
- Onderzoekers streven naar goedkope, efficiënte technologieën voor waterstofopwekking
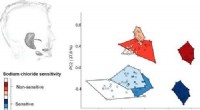
- Speekseleiwitten kunnen verklaren waarom sommige mensen te veel zout gebruiken
- Een verborgen elektronische overgang van S0 naar Tn in moleculen die zware atomen bevatten

- Een bioplastic dat beschermt tegen UV-straling

 Muzikaal erfgoed klonen in de toonsoort 3D
Muzikaal erfgoed klonen in de toonsoort 3D Bevatten organische verbindingen altijd stikstof?
Bevatten organische verbindingen altijd stikstof?  Wat is bodem Genesis?
Wat is bodem Genesis?  Wat zijn enkele niet -voorbeelden van elektrische energie?
Wat zijn enkele niet -voorbeelden van elektrische energie?  Gewoon een orkaan van categorie 1? Laat je niet misleiden door het aantal:het kan verwoestender zijn dan Cat 5
Gewoon een orkaan van categorie 1? Laat je niet misleiden door het aantal:het kan verwoestender zijn dan Cat 5  NASA test parachutesysteem voor landend ruimtevaartuig op Mars
NASA test parachutesysteem voor landend ruimtevaartuig op Mars Een nieuwe light-sheet microscopie-eenheid zorgt voor een groter gezichtsveld en minder fotoschade
Een nieuwe light-sheet microscopie-eenheid zorgt voor een groter gezichtsveld en minder fotoschade Hoe gebruiken robotica -ingenieurs wetenschappelijke notatie?
Hoe gebruiken robotica -ingenieurs wetenschappelijke notatie?
- Elektronica
- Biologie
- Zonsverduistering
- Wiskunde
- French | Italian | Spanish | Portuguese | Swedish | German | Dutch | Danish | Norway |

-
Wetenschap © https://nl.scienceaq.com

