
Wetenschap
Wat is de beperkende reactant wanneer 3,00 mol calcium wordt gereageerd met 8,00 water in de volgende vergelijking?
1. Evenwichtige chemische vergelijking:
De reactie tussen calcium (Ca) en water (H₂o) produceert calciumhydroxide (Ca (OH) ₂) en waterstofgas (H₂):
Ca + 2h₂o → ca (oh) ₂ + h₂
2. Mol -verhouding:
De gebalanceerde vergelijking laat zien dat 1 mol calcium reageert met 2 mol water.
3. Bereken mol water nodig:
Omdat we 3,00 mol calcium hebben, hebben we nodig:
3,00 mol Ca × (2 mol H₂o / 1 mol ca) =6,00 mol H₂o
4. Vergelijk het benodigde water met beschikbaar water:
We hebben 6,00 mol water nodig, maar we hebben slechts 8,00 mol water. Dit betekent dat we genoeg water hebben.
5. Beperkende reactant:
Omdat we voldoende water hebben en niet genoeg calcium, is calcium de beperkende reactant .
 Onderzoekers ontdekken de reden waarom molratten zich niet bewust zijn van zure pijn
Onderzoekers ontdekken de reden waarom molratten zich niet bewust zijn van zure pijn  Zijn alle stoffen vast bij 20 graden Celsius?
Zijn alle stoffen vast bij 20 graden Celsius?  Studie onthult vormingsmechanisme van eerste koolstof-koolstofbinding in MTO-proces
Studie onthult vormingsmechanisme van eerste koolstof-koolstofbinding in MTO-proces Nieuwe inzichten in een oud medicijn:wetenschappers ontdekken waarom aspirine zo goed werkt
Nieuwe inzichten in een oud medicijn:wetenschappers ontdekken waarom aspirine zo goed werkt  Wat is de formule voor aluminium en chloor?
Wat is de formule voor aluminium en chloor?
 De waterkringloop wordt intensiever naarmate het klimaat warmer wordt, meer hevige stormen en overstromingen als gevolg
De waterkringloop wordt intensiever naarmate het klimaat warmer wordt, meer hevige stormen en overstromingen als gevolg Wat zijn de drie belangrijkste klimaatzones van de aarde?
Wat zijn de drie belangrijkste klimaatzones van de aarde?  Welk ecosysteem is Antarctica?
Welk ecosysteem is Antarctica?  Is koolstof het gewas van de toekomst?
Is koolstof het gewas van de toekomst? Wat is de top 3 van natuurlijke hulpbronnen in de VS?
Wat is de top 3 van natuurlijke hulpbronnen in de VS?
Hoofdlijnen
- Wat is Fredderick Griffith -hypothese?
- Nieuwe onderzoeksaanpak:onderzoek naar het mondgevoel van voedsel met een microscoop
- Welke van de klassen RNA -moleculen bevat genetische informatie van kern omdat het nodig is voor de constructie van een eiwit?
- Wat betekent het om kenmerken of eigenschappen te fokken?
- Waar komen grondstoffen vandaan in planten?
- Waar staat de brief e voor in de wetenschap?
- Wat zijn de 3 speciale relaties tussen organismen in een gemeenschap?
- Welk celorganel regelt de synthese van enzymen?
- Een gen is recessief wanneer?
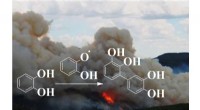
- Bruine koolstof van aromatische verontreinigende stoffen wordt uitgestoten tijdens verbranding en bosbranden
- Moleculaire simulaties laten zien hoe medicijnen belangrijke receptoren blokkeren

- Microcapsules voor gerichte toediening van medicijnen, geïnspireerd op Russische pelmeni

- Een nieuwe benadering om een moeilijk kankerdoelwit te drogeren
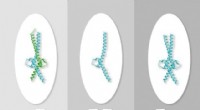
- Orde brengen in chaotische bubbels kan mijnbouw duurzamer maken

 Wat is dodecylbenzenesulfonaat?
Wat is dodecylbenzenesulfonaat?  Als sterren te dicht bij elkaar komen, ze werpen interstellaire kometen en asteroïden uit
Als sterren te dicht bij elkaar komen, ze werpen interstellaire kometen en asteroïden uit Hoe kleine waterdruppeltjes ontstaan, kan een grote impact hebben op klimaatmodellen
Hoe kleine waterdruppeltjes ontstaan, kan een grote impact hebben op klimaatmodellen  Wie heeft de golflengte ontdekt?
Wie heeft de golflengte ontdekt?  Archeologen dringen er bij Albanië op aan om onderwatererfgoed te beschermen
Archeologen dringen er bij Albanië op aan om onderwatererfgoed te beschermen Zwaartekrachtruis interfereert met het bepalen van de coördinaten van verre bronnen
Zwaartekrachtruis interfereert met het bepalen van de coördinaten van verre bronnen Waarom is elektriciteit niet hernieuwbaar?
Waarom is elektriciteit niet hernieuwbaar?  Wat betekent klimaatregio's?
Wat betekent klimaatregio's?
- Elektronica
- Biologie
- Zonsverduistering
- Wiskunde
- French | Italian | Spanish | Portuguese | Swedish | German | Dutch | Danish | Norway |

-
Wetenschap © https://nl.scienceaq.com

