
Wetenschap
Wat is geen manier om de hydroxide- en hydroniumionconcentraties in zuiver water bij 25 Celsius uit te drukken?
Key Concepts
* Neutrale oplossing: Zuiver water is neutraal, wat betekent dat het gelijke concentraties hydronium (H₃o⁺) en hydroxide (OH⁻) ionen heeft.
* kw (constante ionenproduct): Bij 25 ° C is het product van de hydronium- en hydroxide -ionenconcentraties een constante (KW) gelijk aan 1,0 x 10⁻¹⁴.
De juiste uitdrukkingen
1. [H₃o⁺] =[oh⁻] =1,0 x 10⁻⁷ m: Dit is de meest gebruikelijke manier om de concentraties uit te drukken. Aangezien KW =[H₃o⁺] [OH⁻] en KW =1,0 x 10⁻¹⁴, zijn beide concentraties gelijk aan de vierkantswortel van KW, die 1,0 x 10⁻⁷ M is
2. poh =ph =7: De pH en POH worden als volgt berekend:
* pH =-log [H₃o⁺]
* poh =-log [oh⁻]
* Sinds [H₃o⁺] =[oh⁻], pH =poh =7.
De onjuiste uitdrukking
De uitdrukking die onjuist is, is degene die de bovenstaande principes tegenspreekt.
Laten we enkele voorbeelden bekijken:
* [H₃o⁺] =1,0 x 10⁻⁵ m en [oh⁻] =1,0 x 10⁻⁹ m: Dit is onjuist omdat het product van deze concentraties 1,0 x 10⁻¹⁴ is, wat consistent is met KW, maar de concentraties zijn niet gelijk.
Samenvattend:
De juiste uitdrukkingen voor hydroxide- en hydroniumionconcentraties in zuiver water bij 25 ° C benadrukken de gelijke concentraties en de constante waarde van KW. De onjuiste uitdrukking zou er een zijn die deze fundamentele principes niet weerspiegelt.
 Onderzoek gaat de uitdaging aan om stedelijke koolstofemissies te meten
Onderzoek gaat de uitdaging aan om stedelijke koolstofemissies te meten Hoe klimaatverandering en geopolitieke instabiliteit kansen kunnen zijn om de gelijkheid in Nieuw-Zeeland te verbeteren
Hoe klimaatverandering en geopolitieke instabiliteit kansen kunnen zijn om de gelijkheid in Nieuw-Zeeland te verbeteren  Hoe kwam de aarde aan haar water?
Hoe kwam de aarde aan haar water?  Kunnen open en eerlijke wetenschappers het vertrouwen van het publiek winnen?
Kunnen open en eerlijke wetenschappers het vertrouwen van het publiek winnen?  Toekomstige oceaansteden hebben groene techniek boven en onder de waterlijn nodig
Toekomstige oceaansteden hebben groene techniek boven en onder de waterlijn nodig
Hoofdlijnen
- Wat zijn bloedstollingseiwitten?
- Hoe bacteriën zwemmen:onderzoekers ontdekken nieuwe mechanismen
- Forensische wetenschapsprojecten voor middelbare scholieren
- Hoe balsemen werkt
- Wat is een voorbeeld van niet -materie die wetenschapper bestudeert?
- Hoe te voorkomen dat de nederige egel voor altijd uit de Britse tuinen en het platteland verdwijnt?
- Wat zorgen voor eiwitten voor de cel?
- Hoe gebruiken planten de voedingsstoffen en water om voedsel of glucose te produceren?
- Wat doet een dihybride kruis van twee contrasterende pure-fok organismen?
- Licht schijnend op recombinatiemechanismen in zonnecelmaterialen
- Onderzoekers ontwikkelen nieuw proces dat afval omzet in voedingssupplementen

- Onderzoekers ontdekken efficiënte en duurzame manier om zout en metaalionen uit water te filteren

- Nieuwe elektrokatalysator voor waterstofproductie met verbeterde faraday-efficiëntie

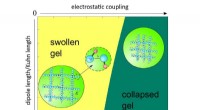
- Onderzoekers ontwikkelen microscopische theorie van polymeergel
 Wat is de textuur van silicium?
Wat is de textuur van silicium?  Hoe de Perseus te vinden Constellation
Hoe de Perseus te vinden Constellation Antiferromagneetroosterarrangementen beïnvloeden faseovergangen
Antiferromagneetroosterarrangementen beïnvloeden faseovergangen De circulaire economie kan ons kapotte watersysteem redden
De circulaire economie kan ons kapotte watersysteem redden Waar gebruiken geologen de zuurtest voor?
Waar gebruiken geologen de zuurtest voor?  Wat is de formule voor goud 1 oxide?
Wat is de formule voor goud 1 oxide?  Wat is de snelheid van 18m in 12 minuten?
Wat is de snelheid van 18m in 12 minuten?  Tropische bossen kunnen binnenkort een belemmering vormen, geen hulp, inspanning voor klimaatverandering
Tropische bossen kunnen binnenkort een belemmering vormen, geen hulp, inspanning voor klimaatverandering
- Elektronica
- Biologie
- Zonsverduistering
- Wiskunde
- French | Italian | Spanish | Portuguese | Swedish | German | Dutch | Danish | Norway |

-
Wetenschap © https://nl.scienceaq.com

