
Wetenschap
Hoe veroorzaakt carbonzuur chemische verwering?
1. Vorming van koolzuur:
* Regenwater absorbeert natuurlijk koolstofdioxide (CO2) uit de atmosfeer.
* Wanneer CO2 oplost in water, vormt het koolzuur (H2CO3), een zwak zuur.
* Dit proces kan worden weergegeven door de volgende vergelijking:
* CO2 + H2O ⇌ H2CO3
2. Reactie met mineralen:
* Carboninezuur, zuur, kan reageren met bepaalde mineralen in rotsen.
* Het meest voorkomende mineraal is calciumcarbonaat (caco3) , dat is het primaire onderdeel van kalksteen en marmer.
* De reactie tussen koolzuur en calciumcarbonaat produceert calciumbicarbonaat (Ca (HCO3) 2), die oplosbaar is in water.
3. Oplossing en verwering:
* Het oplosbare calciumbicarbonaat wordt weggelaten door het water, waardoor de rots effectief oplost.
* Dit proces verzwakt de rotsstructuur, wat leidt tot zijn afbraak.
* De chemische vergelijking voor deze reactie is:
* CACO3 + H2CO3 ⇌ CA (HCO3) 2
4. Vorming van grotten en zinkgaten:
* Gedurende lange periodes kan carbonatatie grote holten creëren in kalksteenformaties, wat resulteert in grotten en zinkgaten.
* Het opgeloste calciumbicarbonaat kan uiteindelijk neerslaan, waardoor stalactieten en stalagmieten in grotten worden gevormd.
Samenvattend is de rol van koolzuur in chemische verwering als volgt:
* Lost mineralen op: Carbonzuur reageert met mineralen, voornamelijk calciumcarbonaat, oplost.
* breekt rotsen af: Dit ontbindingsproces verzwakt de rotsstructuur, wat leidt tot de uitsplitsing ervan.
* Creëert functies: Na verloop van tijd kan carbonatatie aanzienlijke geologische kenmerken veroorzaken, zoals grotten, zinkgaten en karstlandschappen.
Carbonatatie levert een belangrijke bijdrage aan chemische verwering, vooral in gebieden met een aanzienlijke regenval en kalkstenen gesteente. Het speelt een cruciale rol bij het vormgeven van het aardoppervlak en het landschappen.
 Veel Afrikaanse landen overstromen, decennia van ontwikkeling riskeren als ze zich niet aanpassen
Veel Afrikaanse landen overstromen, decennia van ontwikkeling riskeren als ze zich niet aanpassen Gemengde naald- en beukenbossen vullen elkaar aan in het gebruik van hulpbronnen, tenzij er weinig regen valt
Gemengde naald- en beukenbossen vullen elkaar aan in het gebruik van hulpbronnen, tenzij er weinig regen valt Hoe zal de wereld omgaan met de aanval van klimaatvluchtelingen in 2050?
Hoe zal de wereld omgaan met de aanval van klimaatvluchtelingen in 2050?  Weer zorgt voor laagste Europese wijnproductie sinds WO II
Weer zorgt voor laagste Europese wijnproductie sinds WO II De risico's voor de Colorado River-reservoirs nemen af na een natte winter, maar uitdagingen op de langere termijn liggen op de loer
De risico's voor de Colorado River-reservoirs nemen af na een natte winter, maar uitdagingen op de langere termijn liggen op de loer
Hoofdlijnen
- Wat maakt een zoogdierzoogdier?
- Clasper-aanhangsels ontdekt in trilobiet uit het midden van het Cambrium vertonen degenkrabachtig paringsgedrag
- Wat is door mensen geïnduceerde ecosysteemafbraak?
- Helpt aminozuren ons om te groeien?
- Wat zijn cellen met en zonder een kern genoemd?
- Wat zijn de organisatieniveaus in een bioom van het grootste tot snalligste?
- Maak kennis met de kleine machines in cellen die virussen afslachten
- Hoe belangrijke genen samenwerken om een gezonde huid te maken
- Hoe is deze niet -metalen groep chorine en jodium?
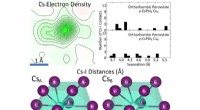
- Chemici lossen de oorsprong van perovskietinstabiliteit op
- Wetenschappers ontdekken dat watermicrodruppels kunnen veranderen in waterstofperoxide wanneer ze condenseren op koude oppervlakken

- Kleine molecule transporteert ijzer in muizen, menselijke cellen om bepaalde vormen van bloedarmoede te behandelen
- Wetenschappers onthullen nieuw dubbel-roamingmechanisme in chemische reactie

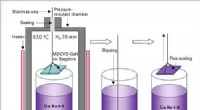
- Ontwikkeling van een nieuwe techniek voor het kweken van hoogwaardige galliumnitridekristallen
 Hoe verandert energie in een zaklamp?
Hoe verandert energie in een zaklamp?  Wat wordt energie opgeslagen in iets fysieks?
Wat wordt energie opgeslagen in iets fysieks?  Nederlandse radioantenne gelanceerd vanaf Chinese basis naar positie achter de maan
Nederlandse radioantenne gelanceerd vanaf Chinese basis naar positie achter de maan Welke beweging is het als je je voet omhoog buigt?
Welke beweging is het als je je voet omhoog buigt?  Geweervuur of plastic zak die knalt? Getraind computermodel weet het verschil
Geweervuur of plastic zak die knalt? Getraind computermodel weet het verschil Het blootleggen van kanker dodelijke koeriers:Nanochains markeren micrometastasen voor vroege diagnose, behandeling
Het blootleggen van kanker dodelijke koeriers:Nanochains markeren micrometastasen voor vroege diagnose, behandeling Foxconn investeert in waterrecyclingsysteem van $30 miljoen
Foxconn investeert in waterrecyclingsysteem van $30 miljoen Een Amerikaanse privacywet kan goed zijn voor Google, maar slecht voor jou (update)
Een Amerikaanse privacywet kan goed zijn voor Google, maar slecht voor jou (update)
- Elektronica
- Biologie
- Zonsverduistering
- Wiskunde
- French | Italian | Spanish | Portuguese | Swedish | German | Dutch | Danish | Norway |

-
Wetenschap © https://nl.scienceaq.com

