
Wetenschap
Welke halogenen zijn gassen bij STP?
De halogenen die gassen zijn bij standaardtemperatuur en druk (STP) zijn:
* fluor (f₂)
* chloor (Cl₂)
Dit is waarom:
* fluor (f₂) en chloor (Cl₂) hebben relatief zwakke intermoleculaire krachten vanwege hun kleinere grootte en lagere moleculaire massa. Deze krachten worden gemakkelijk overwonnen bij kamertemperatuur en druk, wat resulteert in hun gasvormige toestand.
De andere halogenen, broom (Br₂) en jodium (I₂), zijn respectievelijk vloeistoffen en vaste stoffen bij STP, vanwege sterkere intermoleculaire krachten.
 Hoe een vaste concentratie te berekenen
Hoe een vaste concentratie te berekenen  Een revolutionair materiaal voor ruimtevaart en neuromorfisch computergebruik
Een revolutionair materiaal voor ruimtevaart en neuromorfisch computergebruik Welke 5 zuren gebruiken we in ons dagelijks leven?
Welke 5 zuren gebruiken we in ons dagelijks leven?  Welk type chemische reactie is dus koolstofverbrandingen in lucht om CO2 te vormen?
Welk type chemische reactie is dus koolstofverbrandingen in lucht om CO2 te vormen?  Welke items worden gebruikt om warmte te verdelen door een bunsenbrander bij het verwarmen van de bodem van smeltkroes?
Welke items worden gebruikt om warmte te verdelen door een bunsenbrander bij het verwarmen van de bodem van smeltkroes?
 Hoe planten hard werken voor de planeet
Hoe planten hard werken voor de planeet Ontbossing en landopruiming eisen hun tol van de Braziliaanse maïsopbrengst
Ontbossing en landopruiming eisen hun tol van de Braziliaanse maïsopbrengst Upgraden van afvalwaterzuivering resulteert in een aanzienlijke vermindering van intersekse vissen
Upgraden van afvalwaterzuivering resulteert in een aanzienlijke vermindering van intersekse vissen Ballonnen het grootste risico op sterfte in zee voor zeevogels
Ballonnen het grootste risico op sterfte in zee voor zeevogels Tijd tussen wereldveranderende vulkanische superuitbarstingen minder dan eerder gedacht
Tijd tussen wereldveranderende vulkanische superuitbarstingen minder dan eerder gedacht
Hoofdlijnen
- Waarom worden genetisch gemodificeerde gewassen gemaakt?
- Hoe gebruiken wetenschappers technologie om hun bevindingen andere wetenschappers te communiceren?
- Wat is de meeste takken van wetenschap?
- The Differences in Fraternal & Paternal Twins
- Welke van deze soorten heeft een langere binding B2 of B2?
- Wat is het doel van wetenschappelijke modellen?
- Wat is het LRAGE -ogran in uw lichaam?
- Sterven bacteriën ooit uit? Nieuw onderzoek zegt ja, groots
- Chinese fruitvlieggenomen onthullen mondiale migraties en herhaalde evolutie
- Groene productie van chemicaliën voor de industrie

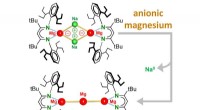
- Onderzoekers rapporteren omgekeerde magnesiumchemie-ontdekking
- Firefly-gen verlicht het vermogen van geoptimaliseerd CRISPR-Cpf1 om het menselijk genoom efficiënt te bewerken

- Hybride enzymkatalysatoren gesynthetiseerd door een de novo benadering voor het uitbreiden van biokatalyse
- Metaalademende bacteriën kunnen elektronica transformeren, biosensoren, en meer

 Welke materialen worden gebruikt om een telescoop te maken?
Welke materialen worden gebruikt om een telescoop te maken?  Een grotere rijkdom aan plantensoorten is misschien niet voldoende om ecosystemen te beschermen tegen de ergste gevolgen van klimaatextremen
Een grotere rijkdom aan plantensoorten is misschien niet voldoende om ecosystemen te beschermen tegen de ergste gevolgen van klimaatextremen Orkaan Laura volgt in de richting van de Amerikaanse Golfkust na het dichtslaan van Haïti
Orkaan Laura volgt in de richting van de Amerikaanse Golfkust na het dichtslaan van Haïti Studie onthult structuur van receptor die betrokken is bij diabetes type 2 en meer
Studie onthult structuur van receptor die betrokken is bij diabetes type 2 en meer Is de koelkast een ICT -tool?
Is de koelkast een ICT -tool?  Kun je de maan en de zon tegelijkertijd zien?
Kun je de maan en de zon tegelijkertijd zien?  Amerikaanse technologiesector ziet slechts bescheiden verlichting in handelsovereenkomst met China
Amerikaanse technologiesector ziet slechts bescheiden verlichting in handelsovereenkomst met China Onderzoeksteam onthult waarom watervocht kwantumkristallen beïnvloedt
Onderzoeksteam onthult waarom watervocht kwantumkristallen beïnvloedt
- Elektronica
- Biologie
- Zonsverduistering
- Wiskunde
- French | Italian | Spanish | Portuguese | Swedish | German | Dutch | Danish | Norway |

-
Wetenschap © https://nl.scienceaq.com

