
Wetenschap
Wat is de verbinding met de kleinste koolstofbinding?
* Bondlengte varieert: Bondlengte is afhankelijk van verschillende factoren, waaronder:
* De soorten atomen betrokken: Een koolstofarbon enkele binding (C-C) is langer dan een dubbele binding van koolstof-koolstofarbon (C =C), die langer is dan een drievoudige binding van koolstof-koolstofarbon (C≡C).
* Hybridisatie: De hybridisatie van de koolstofatomen beïnvloedt de bindingslengte. SP3 gehybridiseerde koolstofatomen hebben bijvoorbeeld langere bindingen dan SP2 gehybridiseerde koolstofatomen.
* De omliggende atomen en groepen: Elektronenintrekkingsgroepen kunnen bindingen verkorten, terwijl elektronendonatiegroepen ze kunnen verlengen.
* specifieke verbindingen nodig: Om te vergelijken, moeten we de specifieke verbindingen kennen waarover u vraagt.
Voorbeeld:
* ethaan (C2H6) heeft een enkele C-C-binding.
* ethyleen (C2H4) heeft een dubbele C =C -binding.
* acetyleen (C2H2) Heeft een drievoudige C≡C -binding.
De C≡C-binding in acetyleen is de kortste, gevolgd door de C =C-binding in ethyleen en vervolgens de C-C-binding in ethaan.
Geef de verbindingen die u wilt vergelijken om een specifieker antwoord te krijgen.
 In welke vloeistoffen zal een ijskubus drijven?
In welke vloeistoffen zal een ijskubus drijven?  Welke twee ingrediënten zijn nodig voor de gisting?
Welke twee ingrediënten zijn nodig voor de gisting?  Wat gebeurt er met waterdamp die condenseert op een oppervlak heeft een temperatuur onder nul graden Celsius?
Wat gebeurt er met waterdamp die condenseert op een oppervlak heeft een temperatuur onder nul graden Celsius?  Doneert of accepteert natrium een elektron?
Doneert of accepteert natrium een elektron?  Wat is het verschil tussen carbonaat- en niet -carbonaathardheid?
Wat is het verschil tussen carbonaat- en niet -carbonaathardheid?
 Gezondheid van bomen gekoppeld aan reactie van vogels op klimaatverandering
Gezondheid van bomen gekoppeld aan reactie van vogels op klimaatverandering Naarmate het klimaat verandert, zal de wereldwijde luchtkwaliteit een deuk oplopen
Naarmate het klimaat verandert, zal de wereldwijde luchtkwaliteit een deuk oplopen Welk deel van het ecosysteem moeten apen vermijden?
Welk deel van het ecosysteem moeten apen vermijden?  Licht werpen op de donkere kant van vervuiling door biomassaverbranding
Licht werpen op de donkere kant van vervuiling door biomassaverbranding Welk effect heeft een afname van zonlicht op het vijver -ecosysteem?
Welk effect heeft een afname van zonlicht op het vijver -ecosysteem?
Hoofdlijnen
- Apen vertonen dramatisch verschillende vroege immuunreacties vergeleken met apen
- Hoe beïnvloedt water het uiterlijk van een groente?
- Zijn schimmelcelnulceus aanwezig of afwezig?
- Wat is nodig voor de evolutie van twee soorten uit subpopulaties, een gemeenschappelijke voorouder?
- Onderzoek toont aan dat een enkel gewas beter kan presteren dan mengsels
- Wat beschrijft het beste waar cellulaire ademhaling?
- Welk type diagram gebruiken wetenschappers om aan te tonen hoe soorten gerelateerd zijn?
- Welk effect is de watercyclus op mensen?
- Hoeveel cellen heeft H2O?
- Moleculaire trillingen benutten om geleidende polymeren te synthetiseren

- Nieuwe plastic biomaterialen kunnen leiden tot hardere, meer veelzijdige medische implantaten
- Nieuwe studie vergroot inzicht in hoe antibioticaresistentie ontstaat
- Chemici onthullen één mechanisme van diwaterstofproductie door stikstofase
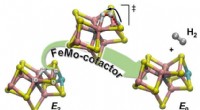
- harde cider, met een scheutje suiker
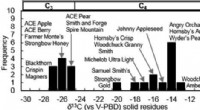
 Wat is een ziekteverwekker die in cel groeit die wordt genoemd?
Wat is een ziekteverwekker die in cel groeit die wordt genoemd?  Perzisch plateau onthuld als cruciaal knooppunt voor vroege menselijke migratie uit Afrika
Perzisch plateau onthuld als cruciaal knooppunt voor vroege menselijke migratie uit Afrika  Waar worden de meeste geothermische bronnen gevonden?
Waar worden de meeste geothermische bronnen gevonden?  Hoe u kunt overstappen van steenkool:4 lessen voor Australië over de hele wereld
Hoe u kunt overstappen van steenkool:4 lessen voor Australië over de hele wereld  Is Malak in de spiraalvormige nebula messier 101 echt?
Is Malak in de spiraalvormige nebula messier 101 echt?  Wat de frequentie van uw loon betekent voor financieel welzijn
Wat de frequentie van uw loon betekent voor financieel welzijn Wat was de favoriete planeet van Neil?
Wat was de favoriete planeet van Neil?  4 wilde manieren waarop wetenschappers CRISPR toepassen
4 wilde manieren waarop wetenschappers CRISPR toepassen
- Elektronica
- Biologie
- Zonsverduistering
- Wiskunde
- French | Italian | Spanish | Portuguese | Swedish | German | Dutch | Danish | Norway |

-
Wetenschap © https://nl.scienceaq.com

