
Wetenschap
Lewis Dot -structuur voor broom en jodium?
1. Bepaal het aantal valentie -elektronen:
* Bromine (Br): Bromine is in groep 17 (ook bekend als groep VIIA), dus het heeft 7 valentie -elektronen.
* jodium (i): Jodium bevindt zich ook in groep 17, dus het heeft ook 7 valentie -elektronen.
2. Vertegenwoordig het atoom met zijn symbool:
* Schrijf het symbool voor het element:"BR" voor broom en "i" voor jodium.
3. Plaats stippen rond het symbool om de valentie -elektronen weer te geven:
* Begin met het plaatsen van één stip aan elke kant van het symbool (boven, onder, links, rechts).
* Combineer vervolgens de resterende stippen aan dezelfde zijden van het symbool.
Lewis Dot -structuren:
Bromine (Br):
`` `
.
:Br:
.
`` `
jodium (i):
`` `
.
:I:
.
`` `
Sleutelpunten:
* De stippen vertegenwoordigen de valentie -elektronen, de elektronen die betrokken zijn bij chemische binding.
* Elke stip vertegenwoordigt één elektron.
* Het maximale aantal stippen rond een atoom is acht, die een volledige buitenste schaal vertegenwoordigen.
* Zowel broom als jodium hebben zeven valentie -elektronen, en hun Lewis -structuren laten zien dat ze één elektron zijn kort voor een volledig octet. Dit maakt ze zeer reactief en zullen waarschijnlijk bindingen vormen om een extra elektron te krijgen.
 Welke structureel verschillend tussen een atoom en ion?
Welke structureel verschillend tussen een atoom en ion?  Wat zijn de chemische elementen van deoxyribose?
Wat zijn de chemische elementen van deoxyribose?  Nieuw covalent organisch raamwerk met boor en fosfor zorgt voor betere connectiviteit
Nieuw covalent organisch raamwerk met boor en fosfor zorgt voor betere connectiviteit Wat is het totale reductiepotentieel van een cel waarin lithium (Li) reduceert en kwik (Hg) oxideert?
Wat is het totale reductiepotentieel van een cel waarin lithium (Li) reduceert en kwik (Hg) oxideert?  Waarom zijn autolichamen niet gemaakt van een metaal met lage dichtheid zoals magnesium?
Waarom zijn autolichamen niet gemaakt van een metaal met lage dichtheid zoals magnesium?
 Alcohol en romantische relaties:een goede of slechte mix?
Alcohol en romantische relaties:een goede of slechte mix?  Systemische verandering in de hele plasticeconomie is nodig om plasticvervuiling in de oceaan een halt toe te roepen
Systemische verandering in de hele plasticeconomie is nodig om plasticvervuiling in de oceaan een halt toe te roepen Grote milieu-uitdaging aangezien microplastics schadelijk zijn voor ons drinkwater
Grote milieu-uitdaging aangezien microplastics schadelijk zijn voor ons drinkwater Siberische regio vecht om permafrost te behouden terwijl planeet opwarmt
Siberische regio vecht om permafrost te behouden terwijl planeet opwarmt Recycling van plastic flessen Carbios haalt donateurs op
Recycling van plastic flessen Carbios haalt donateurs op
Hoofdlijnen
- Wat is Bryophyllum?
- Hoe reproduceert een lionfish zich?
- Wie is wetenschappers?
- Wat is aerobe fosforylering?
- Wat zijn voorbeelden van homozygote dominanten?
- Onderzoekers brachten twee jaar door in diepe ondergrondse grotten om dit buitengewone fossiel aan het licht te brengen
- Wat zijn de belangrijkste groepen domein archaea?
- Waarom is seksueel gedrag tussen mensen van hetzelfde geslacht tijdens de evolutie blijven bestaan?
- Wat is de evolutietheorie door natuurlijke selectie?
- (Re)generatie volgende:nieuwe strategie om steigers te ontwikkelen voor regeneratie van gewrichtsweefsel

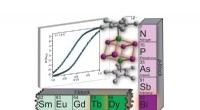
- Onderzoekers maken een magneet gemaakt van één molecuul
- Hout gebruiken in elektroden voor duurzamer, duurzame wearables

- Verbeteren van de samenstelling van stralingsbeschermingsbrillen

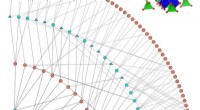
- Een nieuw paradigma van materiaalidentificatie op basis van grafentheorie
 Met welke elementen kan uranium combineren om een verbinding te vormen?
Met welke elementen kan uranium combineren om een verbinding te vormen?  Kristallen kunnen helpen verborgen Kilauea-vulkaangedrag te onthullen
Kristallen kunnen helpen verborgen Kilauea-vulkaangedrag te onthullen Hoe kan dierenafval als energie worden gebruikt?
Hoe kan dierenafval als energie worden gebruikt?  Vindt zink gemakkelijk in brand?
Vindt zink gemakkelijk in brand?  Op welke twee manieren zijn ijzer en koolstof verschillend?
Op welke twee manieren zijn ijzer en koolstof verschillend?  Wat zijn fossielen en fossiele brandstoffen?
Wat zijn fossielen en fossiele brandstoffen?  Leg uit hoe graniet kwartsiet wordt?
Leg uit hoe graniet kwartsiet wordt?  Verweringsproces van graniet
Verweringsproces van graniet
- Elektronica
- Biologie
- Zonsverduistering
- Wiskunde
- French | Italian | Spanish | Portuguese | Swedish | German | Dutch | Danish | Norway |

-
Wetenschap © https://nl.scienceaq.com

