
Wetenschap
Waarom heeft aluminiumoxide een hoog smeltpunt?
* Sterke ionische bindingen: Aluminiumoxide is een zeer ionische verbinding, wat betekent dat het sterke elektrostatische aantrekkingskracht vormt tussen de positief geladen aluminiumionen (Al³⁺) en de negatief geladen oxide -ionen (O²⁻). Deze sterke bindingen vereisen een aanzienlijke hoeveelheid energie om te breken, vandaar het hoge smeltpunt.
* Gigantische ionische roosterstructuur: Aluminiumoxide vormt een gigantische driedimensionale roosterstructuur, waarbij elk aluminiumion wordt omgeven door zes oxide-ionen en vice versa. Dit uitgebreide netwerk van sterke ionische bindingen draagt verder bij aan het hoge smeltpunt.
* High Lattice Enthalpy: De roostertealpie is de energie die nodig is om één mol van een ionische verbinding in zijn gasvormige ionen uit elkaar te breken. De hoge rooster enthalpie van aluminiumoxide geeft de sterkte aan van de ionische bindingen die het kristal bij elkaar houden.
* Hoog elektronegativiteitsverschil: Aluminium en zuurstof hebben een significant elektronegativiteitsverschil, wat leidt tot zeer polaire bindingen en sterke ionische interacties.
Samenvattend draagt de combinatie van sterke ionische bindingen, een gigantische ionische roosterstructuur, enthalpie met een hoog rooster en het grote elektronegativiteitsverschil tussen aluminium en zuurstof allemaal bij aan het uitzonderlijk hoge smeltpunt van aluminiumoxide.
 Wat is de moleculaire massa van H2CO3?
Wat is de moleculaire massa van H2CO3?  Wat ontstaat er door zwaveldioxide als het reageert met waterdruppeltjes in de lucht?
Wat ontstaat er door zwaveldioxide als het reageert met waterdruppeltjes in de lucht?  Waarom reageert magnesiummetaal met een kopersulfaatoplossing terwijl het geen oplossing is?
Waarom reageert magnesiummetaal met een kopersulfaatoplossing terwijl het geen oplossing is?  Wat is de evenwichtige vergelijking voor de reactie van calcicumnitraat en natriumhydroxide?
Wat is de evenwichtige vergelijking voor de reactie van calcicumnitraat en natriumhydroxide?  Wat is de balansformule voor hydrobromzuur en magnesiumsulfiet?
Wat is de balansformule voor hydrobromzuur en magnesiumsulfiet?
 Wetenschappers waarschuwen voor de sociale en ecologische risico's van de energietransitie
Wetenschappers waarschuwen voor de sociale en ecologische risico's van de energietransitie Afbeelding:Copernicus Sentinel-3A-satelliet kijkt naar Harvey
Afbeelding:Copernicus Sentinel-3A-satelliet kijkt naar Harvey De rol van kelpbossen bij het verminderen van de klimaatverandering wordt bedreigd
De rol van kelpbossen bij het verminderen van de klimaatverandering wordt bedreigd Bestrijding van zwavelzuurcorrosie bij afvalwaterzuiveringsinstallaties
Bestrijding van zwavelzuurcorrosie bij afvalwaterzuiveringsinstallaties Review toont unieke zuidwestelijke estuaria
Review toont unieke zuidwestelijke estuaria
Hoofdlijnen
- Hoe zorgwekkend is de verspreiding van de vogelgriep naar melkkoeien? Dit is wat experts zeggen
- Wat is het doel van het vormen van een wetenschappelijke hypothese?
- Op welke manier heeft de vorm van een molecuul invloed op hoe is betrokken bij het levenssysteem?
- Waarom maken ananas-enzymen de biefstuk mals – en je tong?
- Waar gaat de koolstof of plantenkoolstof heen als het sterft?
- Wat zijn glucosemoleculen vergelijkbaar met?
- Wat zijn de subeenheden van DNA?
- Vier hoofdelementen gevonden in een levend organisme?
- DNA uit fossiele eierschalen onthult hoe uitgestorven olifantsvogels leefden
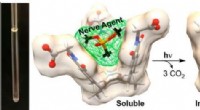
- Giftige verbindingen opsluiten met moleculaire manden
- Autonome zelfgenezing gezien in piëzo-elektrische moleculaire kristallen

- Een nieuw antiseizure-doelwit?

- Kleine borstels die oppervlakken glad maken, werken mogelijk niet zoals bedoeld, studie vondsten

- Gevonden:de heilige graal van katalyse:methaan omzetten in methanol onder omgevingsomstandigheden met behulp van licht

 Wat gebeurt er met een object in vrije val als het terminale snelheid bereikt?
Wat gebeurt er met een object in vrije val als het terminale snelheid bereikt?  Hoe kan een raket zijn brandstof in de ruimte verbranden?
Hoe kan een raket zijn brandstof in de ruimte verbranden?  Onderzoek onderzoekt energie- en landgebruikspraktijken op Amerikaanse golfbanen
Onderzoek onderzoekt energie- en landgebruikspraktijken op Amerikaanse golfbanen  Ingenieurs die geluidsgolven gebruiken om met meer stabiliteit en gemak door big data te zoeken
Ingenieurs die geluidsgolven gebruiken om met meer stabiliteit en gemak door big data te zoeken Welke landvormen vormen hoge vlaktes?
Welke landvormen vormen hoge vlaktes?  Vraag en antwoord met een juridisch expert:wanneer een Tesla op de automatische piloot iemand doodt, wie is dan verantwoordelijk?
Vraag en antwoord met een juridisch expert:wanneer een Tesla op de automatische piloot iemand doodt, wie is dan verantwoordelijk? Wat zijn de belangrijkste bronnen van chloorradicalen?
Wat zijn de belangrijkste bronnen van chloorradicalen?  Wetenschappers maken 's werelds kleinste koelkast
Wetenschappers maken 's werelds kleinste koelkast
- Elektronica
- Biologie
- Zonsverduistering
- Wiskunde
- French | Italian | Spanish | Portuguese | Swedish | German | Dutch | Danish | Norway |

-
Wetenschap © https://nl.scienceaq.com

