
Wetenschap
Wanneer de vergelijking voor volledige verbranding van één mol C3H7OH is gevormd coëfficiënt is zuurstof?
Onevenwichtige vergelijking:
C3H7OH + O2 → CO2 + H2O
het balanceren van de vergelijking:
1. koolstof (c): Er zijn 3 koolstofatomen aan de linkerkant en 1 rechts. Vermenigvuldig CO2 met 3:
C3H7OH + O2 → 3CO2 + H2O
2. waterstof (H): Er zijn 8 waterstofatomen aan de linkerkant en 2 rechts. Vermenigvuldig H2O met 4:
C3H7OH + O2 → 3CO2 + 4H2O
3. zuurstof (O): Er zijn 3 zuurstofatomen aan de linkerkant en 10 aan de rechterkant. Vermenigvuldig o2 met 9/2:
C3H7OH + 9/2 O2 → 3CO2 + 4H2O
4. Hele getallencoëfficiënten: Aangezien we meestal hele getalcoëfficiënten gebruiken, vermenigvuldigt u de hele vergelijking met 2 om van de breuk af te komen:
2C3H7OH + 9O2 → 6CO2 + 8H2O
Antwoord: De coëfficiënt voor zuurstof in de gebalanceerde vergelijking is 9 .
 Waarom overtollig oplosmiddel dat wordt gebruikt in achtertitratie?
Waarom overtollig oplosmiddel dat wordt gebruikt in achtertitratie?  Wat is de dichtheid van CO2 -gas bij STP?
Wat is de dichtheid van CO2 -gas bij STP?  Waarom bewegen zoutzuurdeeltjes sneller dan ammoniakdeeltjes?
Waarom bewegen zoutzuurdeeltjes sneller dan ammoniakdeeltjes?  Welke legeringen worden gevormd door de combinatie van co -pper en zink?
Welke legeringen worden gevormd door de combinatie van co -pper en zink?  Geef je twee voorbeelden van fysische en chemische verandering met water?
Geef je twee voorbeelden van fysische en chemische verandering met water?
 Hoe landschapsplanten impact hebben op de ecologische voetafdruk
Hoe landschapsplanten impact hebben op de ecologische voetafdruk  Beschrijf het Green House -effect en op het klimaat?
Beschrijf het Green House -effect en op het klimaat?  Voorgeschreven verbranding niet zo schadelijk als eerder werd gedacht
Voorgeschreven verbranding niet zo schadelijk als eerder werd gedacht Bossen in hittegolven:Nieuw onderzoek laat zien hoe bomen omgaan met extreme hitte
Bossen in hittegolven:Nieuw onderzoek laat zien hoe bomen omgaan met extreme hitte  Nieuwe studie:Snowpack-niveaus tonen dramatische daling in westerse staten
Nieuwe studie:Snowpack-niveaus tonen dramatische daling in westerse staten
Hoofdlijnen
- Hoe poliepen van de maankwallen virale aanvallen op hun microbioom afweren
- Hoe profiteert virus van het plaatsen van hun genetische materiaal in een gastheercel?
- Celsignalen die wondgenezing in gang zetten zijn verrassend complex
- Wat zijn de functies van mitochondrion in plantencel?
- Wat is glyconeogenis?
- De meest voorkomende cellen die in bindweefsels worden gevonden, worden genoemd?
- Waarom zien we geen robotbeschavingen die zich snel uitbreiden over het universum?
- Hoe telomeren werken
- Voorspelling (biologie): definitie, soorten en voorbeelden
- Ingenieurs ontdekken nieuwe rol van water bij productie van hernieuwbare brandstoffen
- Het is een kwestie van hellingen

- Onderzoek vindt ernstige problemen met forensische software

- Chemici ontwikkelen hydrogelsnaren met behulp van verbindingen die in zeedieren worden gevonden
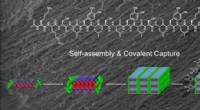
- Wetenschappers ontwikkelen onzichtbare anti-namaaketiketten

 's Werelds grootste ijskap is kwetsbaarder voor de opwarming van de aarde dan wetenschappers eerder dachten
's Werelds grootste ijskap is kwetsbaarder voor de opwarming van de aarde dan wetenschappers eerder dachten Hoe de lengte van de diagonale lijn van een vierkant te meten
Hoe de lengte van de diagonale lijn van een vierkant te meten  Hoe sterrenstelsels afsterven:nieuwe inzichten in het uitdoven van stervorming
Hoe sterrenstelsels afsterven:nieuwe inzichten in het uitdoven van stervorming  Uit welke delen bestaat een steen?
Uit welke delen bestaat een steen?  Wat is de naam voor het proces van scheiding 2 vloeistoffen?
Wat is de naam voor het proces van scheiding 2 vloeistoffen?  Veranderende veerkracht van oceanen tegen klimaatverandering
Veranderende veerkracht van oceanen tegen klimaatverandering Nieuw onderzoek onderzoekt de ervaring van geracialiseerde gemeenschappen tijdens COVID-19
Nieuw onderzoek onderzoekt de ervaring van geracialiseerde gemeenschappen tijdens COVID-19 Wat is de edelsteensteen voor Steenbok?
Wat is de edelsteensteen voor Steenbok?
- Elektronica
- Biologie
- Zonsverduistering
- Wiskunde
- French | Italian | Spanish | Portuguese | Swedish | German | Dutch | Danish | Norway |

-
Wetenschap © https://nl.scienceaq.com

