
Wetenschap
Welk atoom is de kleinste onder lithium en fluor?
Dit is waarom:
* Atomische straal: Atomaire straal verwijst naar de afstand tussen de kern van een atoom en de buitenste elektronenschil. Fluor heeft een kleinere atoomradius dan lithium.
* Nucleaire lading: Fluor heeft een hogere nucleaire lading (meer protonen in de kern) dan lithium. Deze sterkere aantrekkingskracht trekt de elektronen dichter bij de kern, wat resulteert in een kleinere atoomradius.
* Elektronenconfiguratie: Zowel lithium als fluor hebben slechts één elektronenschil. Fluor heeft echter meer protonen, waardoor de kern positiever wordt geladen en de elektronen dichterbij trekken.
Daarom maakt de kleinere atoomradius van fluor het het kleinere atoom.
Hoofdlijnen
- Hoe naamsverandering de carrière van een vrouwelijke onderzoeker kan beïnvloeden
- Wat maakt een plant als voedsel?
- Waar zijn ribosomen op geconstrueerd?
- Menselijk genoom DNA-sequentietypen
- Ideeën voor de dingen Kinderen kunnen met een microscoop bekijken
Kinderen zijn vaak nieuwsgierig naar de wereld om hen heen. Een manier om deze nieuwsgierigheid aan te moedigen, is om ze een manier te bieden om de natuur op een nieuwe en intensiev
- Wat zijn organismen die afval en dood afbreken?
- Team bekijkt hoe eiwitten elkaar ontmoeten op het celmembraan
- Welk dier begint met D moet carnivoren zijn?
- Bijdrage van celstudie door Robert Hooke?
- Elektrostatisch gecontroleerde oppervlakterandvoorwaarden in nematische vloeibare kristallen en colloïden

- Chemici ontwikkelen een veelbelovende methode voor medicijnsynthese
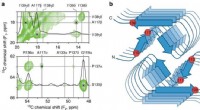
- Onderzoekers onderzoeken hersenziekte-veroorzakende eiwitten op atomair niveau
- Onderzoekers ontwikkelen techniek om koolstofdioxide en methaan te hergebruiken

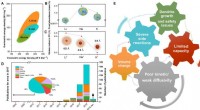
- Onderzoekers schetsen de huidige stand van zaken in de technologie van kalium-ionbatterijen
 Hoe kunstmatige harten werken
Hoe kunstmatige harten werken  Fossiele of anorganische structuur? Wetenschappers graven in vroege levensvormen
Fossiele of anorganische structuur? Wetenschappers graven in vroege levensvormen Wanneer elektromagnetische straling door de ruimte reist?
Wanneer elektromagnetische straling door de ruimte reist?  μkiss:een nieuwe methode voor het nauwkeurig afleveren van nanodeeltjes en kleine moleculen aan individuele cellen
μkiss:een nieuwe methode voor het nauwkeurig afleveren van nanodeeltjes en kleine moleculen aan individuele cellen  Studie:Bewoners verlieten grote metro's tijdens pandemie voor familie
Studie:Bewoners verlieten grote metro's tijdens pandemie voor familie Waarom is koolstof zo belangrijk voor organische verbindingen?
Waarom is koolstof zo belangrijk voor organische verbindingen?  Studie komt dichterbij met bijna-doodervaringen
Studie komt dichterbij met bijna-doodervaringen Facebook-exec ontkent zijn eigen provocerende memo
Facebook-exec ontkent zijn eigen provocerende memo
- Elektronica
- Biologie
- Zonsverduistering
- Wiskunde
- French | Italian | Spanish | Portuguese | Swedish | German | Dutch | Danish | Norway |

-
Wetenschap © https://nl.scienceaq.com


