
Wetenschap
Waarom is niet juist om te spreken van natriumchloridemolecuul?
* ionische binding: Natriumchloride wordt gevormd door de elektrostatische aantrekkingskracht tussen positief geladen natriumionen (Na+) en negatief geladen chloride-ionen (Cl-). Deze ionen zijn gerangschikt in een kristalrooster, zonder afzonderlijke, individuele moleculen.
* Geen discrete eenheden: In tegenstelling tot moleculen, die samen worden gehouden door covalente bindingen, missen ionische verbindingen discrete eenheden. De ionen herhalen continu in een driedimensionale structuur.
* Formule -eenheid: De formule NaCl vertegenwoordigt de eenvoudigste verhouding van ionen in het kristalrooster, bekend als de formule -eenheid.
Samenvattend, terwijl we de term "natriumchloride" gebruiken alsof het een molecuul is, is het nauwkeuriger om het een ionische verbinding te noemen met een formule -eenheid van NaCl.
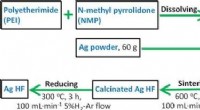
 Licht werpen op perovskiethydriden met behulp van een nieuwe depositietechniek
Licht werpen op perovskiethydriden met behulp van een nieuwe depositietechniek  Is aluminiumchloride een sterke of zwakke elektrolyt?
Is aluminiumchloride een sterke of zwakke elektrolyt?  Snelheidsvoorspelling voor homogene nucleatie van methaanhydraat
Snelheidsvoorspelling voor homogene nucleatie van methaanhydraat Balansvergelijking van natriumchloride met calciumnitraat?
Balansvergelijking van natriumchloride met calciumnitraat?  Hoeveel fluoratomen zijn er in elk molecuul Disulfur decafluoride?
Hoeveel fluoratomen zijn er in elk molecuul Disulfur decafluoride?
 In welk klimaat leeft een nijlpaard?
In welk klimaat leeft een nijlpaard?  Hoe satellietgegevens leidden tot een doorbraak voor de giftige algenbloei in Lake Erie
Hoe satellietgegevens leidden tot een doorbraak voor de giftige algenbloei in Lake Erie Hoe 'ethische beïnvloeders' hun publiek betrekken bij het redden van de planeet
Hoe 'ethische beïnvloeders' hun publiek betrekken bij het redden van de planeet  De glaciale geschiedenis van het westelijke noordpoolgebied begrijpen
De glaciale geschiedenis van het westelijke noordpoolgebied begrijpen Klimaatcrisis:de hoop op een grens van 1,5°C levend houden is van vitaal belang om wereldwijde actie aan te zwengelen
Klimaatcrisis:de hoop op een grens van 1,5°C levend houden is van vitaal belang om wereldwijde actie aan te zwengelen
Hoofdlijnen
- Welk organisme dat vandaag leeft, is gerelateerd aan de trilobiet?
- Wat zijn niet-edelbare planten?
- Hebben plantencellen nucleaire membranen?
- Wat is basis voor evolutie door natuurlijke selectie?
- Birdsong onthult zeldzame hybride koppeling die 10 miljoen jaar in de maak is
- Is de wetenschap slaap aan het uitfaseren?
- Hoe konden gelelektroforese worden gebruikt om te zien of een genetische modificatie -experiment succesvol was?
- Hoe de darmen aan hun villi kwamen:bij het vergelijken van soorten onderzoeken onderzoekers een proces dat zij 'vervilting' noemen
- Wat kan er gebeuren met menselijke bloedcellen als ze in een beker van zout water worden geplaatst?
- Onderzoekers stellen een nieuwe methode voor om de elektrokatalytische omzetting van koolstofdioxide te verbeteren
- Decontaminatie van water met zware metalen met behulp van eiwit uit plantaardig afval
- Het bereik van therapeutische antilichamen vergroten
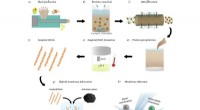
- Nieuwe supramoleculaire copolymeren aangedreven door zelfsortering van moleculen

- Wederopstanding van quasikristallen:bevindingen maken een exotisch materiaal commercieel levensvatbaar

 Equatoriale luchtmassakarakteristieken
Equatoriale luchtmassakarakteristieken Wat gebeurt er als een atoom energie verliest?
Wat gebeurt er als een atoom energie verliest?  Wat is de studie van erfelijkheid?
Wat is de studie van erfelijkheid?  Zal de laatste wraakactie van Steve Jobs Google achtervolgen?
Zal de laatste wraakactie van Steve Jobs Google achtervolgen?  Hoe beïnvloeden zuren en basen groene planten?
Hoe beïnvloeden zuren en basen groene planten?  Wat zijn feiten over de dubbele ster?
Wat zijn feiten over de dubbele ster?  Is het belangrijkste gas in de Venusiaanse atmosfeer en ook een ondergeschikt onderdeel van atmosferen Earth Mars?
Is het belangrijkste gas in de Venusiaanse atmosfeer en ook een ondergeschikt onderdeel van atmosferen Earth Mars?  Houden niet-leuke schimmels kunstmest van planten?
Houden niet-leuke schimmels kunstmest van planten?
- Elektronica
- Biologie
- Zonsverduistering
- Wiskunde
- French | Italian | Spanish | Portuguese | Swedish | German | Dutch | Danish | Norway |

-
Wetenschap © https://nl.scienceaq.com

