
Wetenschap
Wat is het product van ammoniumchloride plus natriumhydroxide?
Hier is de evenwichtige chemische vergelijking:
nH₄cl (aq) + NaOH (aq) → nH₃ (g) + h₂o (l) + NaCl (aq)
Hier is een uitsplitsing van de reactie:
* ammoniumchloride (NH₄CL) is een zout dat oplost in water om ammoniumionen (NH₄⁺) en chloride -ionen (CL⁻) te vormen.
* Natriumhydroxide (NaOH) is een sterke basis die oplost in water om natriumionen (Na⁺) en hydroxide -ionen (OH⁻) te vormen.
* Wanneer deze oplossingen worden gemengd, reageren de ammoniumionen (NH₄⁺) met de hydroxide -ionen (OH⁻) om ammoniak (NH₃) en water (H₂o) te produceren. Ammoniak is een gas, dus het zal uit de oplossing worden vrijgegeven.
* De resterende natriumionen (Na⁺) en chloride -ionen (CL⁻) combineren om natriumchloride (NaCl) te vormen, die in de oplossing opgelost blijft.
Belangrijke opmerking: Deze reactie is een evenwichtsreactie. De geproduceerde ammoniak zal ontsnappen als een gas, waardoor de reactie aan de rechterkant wordt gestimuleerd, wat de vorming van producten bevordert.
 Hoeveel koolstofatomen zitten er in een molecuul als het 12 zuurstofatomen heeft?
Hoeveel koolstofatomen zitten er in een molecuul als het 12 zuurstofatomen heeft?  Wat is hematiet-ijzerglans ijzeroxide?
Wat is hematiet-ijzerglans ijzeroxide?  Studie toont potentieel voor milieuvriendelijke vervanging van plastic
Studie toont potentieel voor milieuvriendelijke vervanging van plastic Supersnel inzicht in mobiele gebeurtenissen
Supersnel inzicht in mobiele gebeurtenissen Wat zijn atomen van verschillende elementen waarvan wordt gezegd dat ze worden genoemd?
Wat zijn atomen van verschillende elementen waarvan wordt gezegd dat ze worden genoemd?
 Hoe de klimaatverandering aan te pakken, voedselzekerheid en landdegradatie
Hoe de klimaatverandering aan te pakken, voedselzekerheid en landdegradatie bijna 4, 500 Amazon-medewerkers dagen bedrijf uit om het voortouw te nemen in beleid inzake klimaatverandering
bijna 4, 500 Amazon-medewerkers dagen bedrijf uit om het voortouw te nemen in beleid inzake klimaatverandering Chemische zonnebrandmiddelen in water kunnen visembryo's beschadigen
Chemische zonnebrandmiddelen in water kunnen visembryo's beschadigen Hoe om te gaan met ecologische en sociale uitdagingen in waterbeheer
Hoe om te gaan met ecologische en sociale uitdagingen in waterbeheer Warmer klimaat leidt tot actuele trends van sociale onrust en massamigratie:studie
Warmer klimaat leidt tot actuele trends van sociale onrust en massamigratie:studie
Hoofdlijnen
- Reviewing over moleculaire geneeskunde onthult de rol van IGF bij kanker en andere proliferatieve ziekten
- Interferentie berekenen
- Waarom is stikstof belangrijk voor levende wezens?
- Welke cellen kunnen door het menselijk oog worden gezien?
- Wat betekent analyseren in de wetenschappelijke methode?
- Hoe wordt microscoop gebruikt om informatie te verzamelen?
- Wat is de wetenschappelijke classificatie van ashwagandha?
- Wat wordt bedoeld met waargenomen genotypen?
- De eieren van amfibieën kunnen gemakkelijk uitdrogen omdat ze?
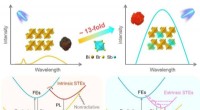
- Ontwikkeling van anorganisch loodvrij perovskiet voor breedbandemissie
- Ontwikkelen van een blokcopolymeer dat veiligere, stabielere batterijen mogelijk maakt

- Reparatie en regeneratie van perifere zenuwen mogelijk met dubbele polymeer hydrogellijm

- Wetenschappers gebruiken katalysatoren om kankercellen van binnenuit te vernietigen
- Veranderingen in suikerachtige moleculen aan het oppervlak helpen kanker uitzaaien

 Onderzoekers laten zien hoe mengsels van biomoleculen communiceren, interageren en zich aanpassen aan hun omgeving
Onderzoekers laten zien hoe mengsels van biomoleculen communiceren, interageren en zich aanpassen aan hun omgeving  Mechanochemische vorming van peptidebindingen achter de oorsprong van het leven
Mechanochemische vorming van peptidebindingen achter de oorsprong van het leven Het ontwikkelen van een veilige, niet-hackbaar netwerk
Het ontwikkelen van een veilige, niet-hackbaar netwerk Wat zou er gebeuren als de zon nooit zou bestaan?
Wat zou er gebeuren als de zon nooit zou bestaan?  Facebook koopt startup die werkt aan mind-control van machines
Facebook koopt startup die werkt aan mind-control van machines Hoe vind je de molaire massa van verbindingen zoals water?
Hoe vind je de molaire massa van verbindingen zoals water?  Conversie van statistisch naar pond
Conversie van statistisch naar pond  Klein, snel, en zeer energiezuinig geheugenapparaat geïnspireerd op lithium-ionbatterijen
Klein, snel, en zeer energiezuinig geheugenapparaat geïnspireerd op lithium-ionbatterijen
- Elektronica
- Biologie
- Zonsverduistering
- Wiskunde
- French | Italian | Spanish | Portuguese | Swedish | German | Dutch | Danish | Norway |

-
Wetenschap © https://nl.scienceaq.com

