
Wetenschap
Wat is de molaire concentratie van 7,25 g zilvernitraat opgelost in oplossing van 100 ml?
1. Vind de molaire massa zilvernitraat (Agno₃):
* Ag:107.87 g/mol
* N:14.01 g/mol
* O:16.00 g/mol (x3 =48,00 g/mol)
Totale molaire massa =107,87 + 14.01 + 48,00 =169,88 g/mol
2. Converteer gram zilvernitraat in mol:
* Mol =(massa in gram) / (molaire massa)
* Mol =7,25 g / 169,88 g / mol =0,0427 mol
3. Converteer milliliter van oplossing naar liters:
* Liters =(milliliter) / 1000
* Liters =100 ml / 1000 =0,1 l
4. Bereken de molaire concentratie (molariteit):
* Molariteit (m) =(mol opgeloste stof) / (liters van oplossing)
* Molariteit =0,0427 mol / 0,1 l = 0,427 m
Daarom is de molaire concentratie van de zilvernitraatoplossing 0,427 m.
Hoofdlijnen
- Wat is de PET -scan een voorbeeld van anatomische terminologie die beschrijft als een?
- Site waar ribosomaal RNA wordt gemaakt?
- Lang gezochte eiwitstructuur kan helpen onthullen hoe 'genschakelaar' werkt (video)
- Wat zou er talrijker zijn in spiercellen dan huidcellen?
- De ontdekking van een mijlpaal verandert de evolutiemarathon in een sprint
- Waarom ontwikkelden complexe organismen die de aarde bewonen?
- Wat is een polygenetische eigenschap?
- Nieuwe studie onderzoekt hoe bacteriën immuniteit verwerven
- Twee fasen van fotosynthese
- Kathodemateriaal gemaakt van organische moleculen verbetert de groene eigenschappen van oplaadbare batterijen
- Zelfherstellend omgekeerd filter opent de deur voor veel nieuwe toepassingen

- Nieuw bewijs toont aan dat de eerste bouwstenen van het leven op aarde misschien rommeliger waren dan eerder werd gedacht

- Een nieuwe manier om kogelvrije vesten te testen

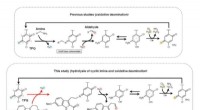
- Onderzoekers kijken naar de natuur om de geheimen van cyclische imine-splitsing te ontrafelen
 Van zwarte gaten tot zand:toepassing van holografische dualiteit op korrelige materie
Van zwarte gaten tot zand:toepassing van holografische dualiteit op korrelige materie Isolatoren met geleidende randen begrijpen
Isolatoren met geleidende randen begrijpen Hoe de Melkweg werkt
Hoe de Melkweg werkt  Wat betekent een onderwerp?
Wat betekent een onderwerp?  Wanneer ontdekte Alfred Wegener de theorie van plaattektoniek?
Wanneer ontdekte Alfred Wegener de theorie van plaattektoniek?  Caltech-onderzoekers ontwerpen een nieuw nanomesh-materiaal
Caltech-onderzoekers ontwerpen een nieuw nanomesh-materiaal Wat is de relatie tussen angstrom en astronomische eenheid?
Wat is de relatie tussen angstrom en astronomische eenheid?  Waarom botsen vogels tegen zonnepanelen?
Waarom botsen vogels tegen zonnepanelen?
- Elektronica
- Biologie
- Zonsverduistering
- Wiskunde
- French | Italian | Spanish | Portuguese | Swedish | German | Dutch | Danish | Norway |

-
Wetenschap © https://nl.scienceaq.com


