
Wetenschap
Waarom is dat het meest actieve metaal van Francium?
* elektropositiviteit: Francium staat onderaan groep 1 (alkali -metalen) op het periodieke tabel. Elementen in deze groep staan bekend als alkali -metalen en ze zijn allemaal zeer reactief. Naarmate je de groep naar beneden gaat, neemt de reactiviteit toe. Dit komt omdat het buitenste elektron (valentie -elektron) verder van de kern komt, waardoor het gemakkelijker is om een positief ion (kation) te verwijderen en te vormen. Francium heeft de grootste atoomstraal van alle alkali -metalen, wat betekent dat het valentie -elektron het verst van de kern is en de minste aantrekkingskracht ervaart.
* Lage ionisatie -energie: Francium heeft de laagste ionisatie -energie van alle elementen. Ionisatie -energie is de energie die nodig is om een elektron uit een atoom te verwijderen. Omdat het valentie -elektron van Francium zwak wordt vastgehouden, kost het heel weinig energie om het te verwijderen. Dit zorgt ervoor dat Francium zeer waarschijnlijk een elektron verliest en een positief ion vormt.
* Hoge elektronegativiteit: Elektronegativiteit is een maat voor het vermogen van een atoom om elektronen aan te trekken. Francium heeft een zeer lage elektronegativiteit, wat betekent dat het een sterke neiging heeft om zijn elektron te verliezen in plaats van er een te krijgen.
Samenvattend: De combinatie van de grote atoomradius van Francium, lage ionisatie -energie en lage elektronegativiteit maakt het het meest reactieve metaal. De neiging om zijn elektron te verliezen leidt gemakkelijk tot zijn zeer reactieve aard. Francium is echter een zeer zeldzaam en radioactief element, waardoor het moeilijk is om de reactiviteit ervan in detail te bestuderen.
 Top EPA-adviseurs dagen al lang bestaande luchtvervuilingswetenschap uit, een bedreiging voor de gezondheid van de Amerikanen
Top EPA-adviseurs dagen al lang bestaande luchtvervuilingswetenschap uit, een bedreiging voor de gezondheid van de Amerikanen Verschillende soorten waterlichamen
Verschillende soorten waterlichamen  Drones gebruikt om aswolken van vulkaan Guatemalteeks te analyseren
Drones gebruikt om aswolken van vulkaan Guatemalteeks te analyseren Welk lichaam gloeit de zon aarde of beide?
Welk lichaam gloeit de zon aarde of beide?  Zwarte zomerbranden in Australië hebben de ozonlaag aangetast:studie
Zwarte zomerbranden in Australië hebben de ozonlaag aangetast:studie
Hoofdlijnen
- Hier ziet u hoe wetenschappers de genetische evolutie van COVID-19 volgen
- Indonesië's selfiesnagende aap uitgeroepen tot Persoon van het Jaar
- De opvallende gele keel van een grasmus? Daar zijn genen voor
- Waarom onderzoekers geïnteresseerd zijn in het gezond houden van (sommige) koraalduivels
- Wat is de suikerfosfaat -ruggengraat van DNA?
- We volgen al 18 jaar vogels in een klein Nigeriaans bos - wat we hebben gevonden en waarom het ertoe doet
- Welk molecuul bindt aan de startreactie van de receptor in cel?
- Wat zijn twee orgaansystemen die het meest betrokken zijn bij groei en regulering?
- Wat zou een arm molecule celweefsel of orgaan zijn?
- Chemici bereiken moleculaire bewerkingsprestatie
- Wetenschappers ontwikkelen een materiaal voor gebruik in stralingstolerante apparaten

- Geneesmiddelen en producten voor persoonlijke verzorging opzuigen uit water

- Video:De chemie achter van kleur veranderende vogels

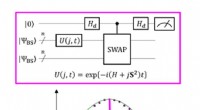
- Spinchemie heroverwegen vanuit een kwantumperspectief
 Hoe is golfenergie afhankelijk van de zon?
Hoe is golfenergie afhankelijk van de zon?  Welke twee energiebronnen voor processen in lithosfeer Hydrosfeer atmosfeer biosfeer?
Welke twee energiebronnen voor processen in lithosfeer Hydrosfeer atmosfeer biosfeer?  Waarom worden lichte golven gebroken aan een grens tussen 2 materialen?
Waarom worden lichte golven gebroken aan een grens tussen 2 materialen?  Evaporatie-experiment voor kinderen bekijken
Evaporatie-experiment voor kinderen bekijken Hoe beïnvloedt de massa en snelheid van een bewegend object zijn momentum?
Hoe beïnvloedt de massa en snelheid van een bewegend object zijn momentum?  Westerse bosbranden:brand in Californië steekt Nevada over
Westerse bosbranden:brand in Californië steekt Nevada over Berekenen van dampkap Velocity
Berekenen van dampkap Velocity Hoe wormen bewegen?
Hoe wormen bewegen?
- Elektronica
- Biologie
- Zonsverduistering
- Wiskunde
- French | Italian | Spanish | Portuguese | Swedish | German | Dutch | Danish | Norway |

-
Wetenschap © https://nl.scienceaq.com

