
Wetenschap
Hoe breng je CO2 plus H2 in evenwicht om CH3OH op te leveren?
De reactie:
De omzetting van koolstofdioxide (CO2) en waterstof (H2) in methanol (CH3OH) staat bekend als de methanolsynthesereactie . Het is een complex proces dat een katalysator vereist (meestal op koper gebaseerd) en hoge druk (meestal 50-100 atm) en matige temperatuur (ongeveer 250 ° C).
De gebalanceerde vergelijking (vereenvoudigd):
CO2 + 3H2 ⇌ CH3OH + H2O
Waarom het geen eenvoudige balans is:
* katalysatoren: De vergelijking weerspiegelt de rol van de katalysator niet. De katalysator is essentieel voor de reactie.
* reactieomstandigheden: De reactie is omkeerbaar en vereist specifieke omstandigheden (temperatuur, druk) om de vorming van methanol te bevorderen.
* Meerdere stappen: Het algemene proces is eigenlijk een reeks stappen met tussenproducten en nevenreacties.
Samenvattend: Hoewel u een vereenvoudigde evenwichtige vergelijking kunt schrijven om de algehele reactie weer te geven, wordt niet volledig de complexiteit van het methanolsyntheseproces vastgelegd.
Sleutelpunten:
* Synthese van methanol is een industrieel belangrijk proces: Het produceert een waardevolle brandstof- en chemische grondstof.
* onderzoek is aan de gang: Wetenschappers onderzoeken continu manieren om de efficiëntie en duurzaamheid van methanolsynthese te verbeteren.
 Wat is de chemische samenstelling van een vlam?
Wat is de chemische samenstelling van een vlam?  Atomaire resolutie-eiwitmodellen onthullen nieuwe details over eiwitbinding
Atomaire resolutie-eiwitmodellen onthullen nieuwe details over eiwitbinding Wat is een chemische reactie waarin het ene element een andere verbinding of twee elementen vervangt die verschillende verbindingen handelen?
Wat is een chemische reactie waarin het ene element een andere verbinding of twee elementen vervangt die verschillende verbindingen handelen?  Karamelkleur is het organisch of anorganisch?
Karamelkleur is het organisch of anorganisch?  Berekening van de druk van waterstofgas
Berekening van de druk van waterstofgas
Hoofdlijnen
- Duiven kunnen zowel ruimte als tijd onderscheiden
- Wat is de pH in enzymenactiviteit?
- Zijn er levende organismen zonder cellen?
- Hoe is deze niet -metalen groep chorine en jodium?
- Waarom laten mensen twee sets tanden groeien? Deze buideldieren herschrijven het verhaal van de tandevolutie
- Wat hebben dominante en recessieve allelen gemeen?
- DNA-studies tonen micro-evolutie aan bij pinguïns
- Hoe verkrijgt Protist energie in schimmel?
- Lymphatic System Science Activities
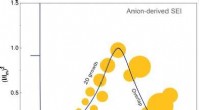
- Anionen en oplosmiddelen sturen kiemvorming en groei van de vaste elektrolyt-interfase
- Een minuut gelijktijdige analyse van scherpte componenten in Kimchi

- Een kleine cirkelvormige racebaan voor licht kan snel afzonderlijke moleculen detecteren

- Kunstmatige antioxidant kan het volgende supplement zijn

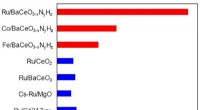
- Efficiënte bottom-up synthese van nieuw perovskietmateriaal voor de productie van ammoniak
 Hoe NASA eenvoudige technologie gebruikt om maanmissies te volgen
Hoe NASA eenvoudige technologie gebruikt om maanmissies te volgen  DNA-apparaten voeren bio-analytische chemie uit in levende cellen
DNA-apparaten voeren bio-analytische chemie uit in levende cellen Wat vervuilt de atmosfeer het meest?
Wat vervuilt de atmosfeer het meest?  Kunstmatige gletsjers als reactie op klimaatverandering?
Kunstmatige gletsjers als reactie op klimaatverandering? Welk model van het universum dat suggereert dat de zon centrum is, werd voor het eerst gebracht?
Welk model van het universum dat suggereert dat de zon centrum is, werd voor het eerst gebracht?  Nanotechnologie geeft groene energie een groene kleur
Nanotechnologie geeft groene energie een groene kleur Filippijnse minister zegt dat Nickelodeon niet kan bouwen op het ongerepte Palawan
Filippijnse minister zegt dat Nickelodeon niet kan bouwen op het ongerepte Palawan Hoe de baan Slope
Hoe de baan Slope
- Elektronica
- Biologie
- Zonsverduistering
- Wiskunde
- French | Italian | Spanish | Portuguese | Swedish | German | Dutch | Danish | Norway |

-
Wetenschap © https://nl.scienceaq.com

