
Wetenschap
Wat is de chemische samenstelling van een vlam?
1. Reactanten:
* brandstof: De stof wordt verbrand. Dit kan een vaste stof zijn zoals hout, een vloeistof zoals kerosine of een gasachtig methaan.
* oxidant: Typisch zuurstof uit de lucht, maar andere oxidatiemiddelen zoals chloor of fluor kunnen ook worden gebruikt.
2. Producten van verbranding:
* waterdamp (H2O): Gevormd wanneer waterstof uit de brandstof reageert met zuurstof.
* koolstofdioxide (CO2): Gevormd wanneer koolstof uit de brandstof reageert met zuurstof.
* stikstof (n2): Stikstof is de meest voorkomende component van lucht en blijft grotendeels ongewijzigd tijdens de verbranding.
* koolmonoxide (CO): Een giftig gas dat wordt geproduceerd wanneer er onvoldoende zuurstof is voor volledige verbranding.
* Andere gassen: Afhankelijk van de brandstof kunnen andere gassen aanwezig zijn, waaronder zwaveldioxide (SO2), roet (fijne koolstofdeeltjes) en onverbrande brandstof.
3. Vrije radicalen:
* zeer reactieve soorten: Dit zijn atomen of moleculen met ongepaarde elektronen, waardoor ze zeer onstabiel en zeer reactief zijn. Voorbeelden zijn waterstofradicalen (H •) en zuurstofradicalen (o •).
4. Ionen en opgewonden soorten:
* opgewonden atomen en moleculen: Dit zijn atomen of moleculen die energie hebben geabsorbeerd en zich in een onstabiele toestand bevinden. Ze stoten licht uit wanneer ze terugkeren naar hun grondtoestand, wat de reden is dat vlammen gloeien.
* ionen: Atomen of moleculen die elektronen hebben verloren of gewonnen en elektrisch geladen worden.
De kleur van een vlam is vaak een indicatie van de temperatuur en de aanwezige elementen. Een blauwe vlam duidt bijvoorbeeld op een zeer hete en schone verbranding met volledige verbranding, terwijl een gele of oranje vlam een koelere temperatuur en onvolledige verbranding met roetvorming aangeeft.
Samenvattend is de chemische samenstelling van een vlam een dynamisch mengsel van reactanten, producten van verbranding, vrije radicalen, ionen en opgewonden soorten. De specifieke componenten en hun relatieve concentraties variëren sterk, afhankelijk van de brandstof- en verbrandingsomstandigheden.
 Onderzoekers bedenken proces om duurzaam rubber te maken, kunststoffen
Onderzoekers bedenken proces om duurzaam rubber te maken, kunststoffen Nieuwe ontdekking van een zo sterke photobase, het verdient de bijnaam super
Nieuwe ontdekking van een zo sterke photobase, het verdient de bijnaam super Spinchemie heroverwegen vanuit een kwantumperspectief
Spinchemie heroverwegen vanuit een kwantumperspectief Welke chemische stof is verantwoordelijk voor de zure snelle eigenschap van Mycobacteria?
Welke chemische stof is verantwoordelijk voor de zure snelle eigenschap van Mycobacteria?  Zakken of bakken? Als het om recycling gaat, is het antwoord ingewikkeld
Zakken of bakken? Als het om recycling gaat, is het antwoord ingewikkeld
 Palmolie:Minder kunstmest en geen herbicide maar dezelfde opbrengst?
Palmolie:Minder kunstmest en geen herbicide maar dezelfde opbrengst? Antimaterie:we hebben ontdekt hoe de zwaartekracht het beïnvloedt. Wat het betekent voor ons begrip van het universum
Antimaterie:we hebben ontdekt hoe de zwaartekracht het beïnvloedt. Wat het betekent voor ons begrip van het universum  Hernieuwde branddreiging leidt tot uittocht naar Australische steden
Hernieuwde branddreiging leidt tot uittocht naar Australische steden Verschillen in hoogte van wolkentop tussen satellieten en grondradar onthuld
Verschillen in hoogte van wolkentop tussen satellieten en grondradar onthuld Satellietgegevens gebruikt om zeeplastic te detecteren
Satellietgegevens gebruikt om zeeplastic te detecteren
Hoofdlijnen
- Eiwittrekken - Leren hoe eiwitten zich daardoor uit elkaar vouwen
- Wetenschappers onthullen superbugs-artillerie
- Hoeveel cellen moeten samen als weefsel tellen?
- Gele erwten laten veelbelovende resultaten zien als basis voor de kaas van morgen
- In een hondenlichaam heeft elke cel 78 chromosomen hoeveel zijn er in spermacellen?
- Hoe zijn zowel vissen als zoogdieren?
- Het belangrijkste orgaan in ons lichaam zijn de hersenen?
- Wat zijn soorten secundaire cellen?
- Is het waar dat planten voedingsstoffen rechtstreeks in fotosynthese gebruiken?
- Transparant keramisch pantser biedt superieure ballistische bescherming ten opzichte van traditionele glaslaminaten

- Thorium-228-aanvoer rijp voor onderzoek naar medische toepassingen

- Geheime berichten verborgen in lichtgevoelige polymeren
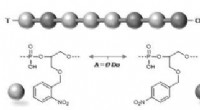
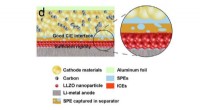
- Onderzoekers ontwerpen dendrietvrije lithiumbatterij
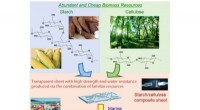
- Onderzoekers maken in water afbreekbaar plastic dat zetmeel en cellulose combineert
 Extreemrechts geweld in Portugal put kracht uit skinhead-wortels - studie
Extreemrechts geweld in Portugal put kracht uit skinhead-wortels - studie Waarom de lente prachtig bloeit (en de klimaatverandering het eerder maakt)
Waarom de lente prachtig bloeit (en de klimaatverandering het eerder maakt)  Wawa geconfronteerd met rechtszaken wegens datalek in al zijn winkels
Wawa geconfronteerd met rechtszaken wegens datalek in al zijn winkels Planten herprogrammeren hun cellen om indringers te bestrijden. Hier is hoe
Planten herprogrammeren hun cellen om indringers te bestrijden. Hier is hoe De kwantumcode kraken:simulaties volgen verstrengelde quarks
De kwantumcode kraken:simulaties volgen verstrengelde quarks  Kun je mij een voorbeeld geven van een continent?
Kun je mij een voorbeeld geven van een continent?  Welke stad heeft deze coördinaten 1s en 37e?
Welke stad heeft deze coördinaten 1s en 37e?  Eerste interstellaire immigrant ontdekt in het zonnestelsel
Eerste interstellaire immigrant ontdekt in het zonnestelsel
- Elektronica
- Biologie
- Zonsverduistering
- Wiskunde
- French | Italian | Spanish | Portuguese | Swedish | German | Dutch | Danish | Norway |

-
Wetenschap © https://nl.scienceaq.com

