
Wetenschap
Het proces waardoor sommige moleculaire verbindingen oplosen in water om ionen te vormen, is?
Hier is een uitsplitsing:
* moleculaire verbindingen worden gevormd door het delen van elektronen tussen atomen (covalente bindingen).
* ionen zijn atomen of groepen atomen die een elektrische lading dragen (positief of negatief).
* ionisatie is het proces waarbij een neutrale molecule elektronen wint of verliest, wat resulteert in de vorming van ionen.
Hoe het werkt in water:
1. Polariteit: Watermoleculen zijn polair, wat betekent dat ze een enigszins positief uiteinde en een enigszins negatief uiteinde hebben als gevolg van de ongelijke delen van elektronen.
2. Aantrekking: Wanneer een polaire moleculaire verbinding water binnenkomt, trekken de positieve en negatieve uiteinden van de watermoleculen de tegengesteld geladen uiteinden van het molecuul aan.
3. Bond breken: De sterke aantrekkingskracht tussen de watermoleculen en de moleculaire verbinding kan de bindingen in het molecuul overwinnen, waardoor deze uit elkaar breekt.
4. ionenvorming: De gebroken fragmenten van het molecuul komen of verliezen elektronen, waardoor ionen worden gevormd.
Voorbeeld:
* waterstofchloride (HCl) is een moleculaire verbinding. Wanneer het oplost in water, ioniseert het om waterstofionen (H+) en chloride-ionen (Cl-) te vormen.
* HCl (G) + H2O (L) → H3O + (aq) + Cl- (aq)
Opmerking: Niet alle moleculaire verbindingen ioniseren in water. Alleen degenen die polaire bindingen hebben en in staat zijn om sterke interacties met watermoleculen te vormen, zullen dit proces ondergaan.
 Analyse van een verbinding bestaande uit ijzer en zuurstof levert 174,86 g Fe op. 75,14 O Wat is de empirische formule voor deze verbinding?
Analyse van een verbinding bestaande uit ijzer en zuurstof levert 174,86 g Fe op. 75,14 O Wat is de empirische formule voor deze verbinding?  Welk zuur is sterker Pepsi of sinaasappelsap?
Welk zuur is sterker Pepsi of sinaasappelsap?  Onderzoekers verbeteren de plasticiteit van keramische materialen bij kamertemperatuur
Onderzoekers verbeteren de plasticiteit van keramische materialen bij kamertemperatuur  Wat is silicagel en waarom vind ik bij elke aankoop kleine pakjes ervan?
Wat is silicagel en waarom vind ik bij elke aankoop kleine pakjes ervan?  Wat is het verschil tussen benzine, kerosine, diesel, enz.?
Wat is het verschil tussen benzine, kerosine, diesel, enz.?
 Primatoloog observeert hoe apen hun gedrag veranderen om de ontbossing te overleven
Primatoloog observeert hoe apen hun gedrag veranderen om de ontbossing te overleven  Snelle opwarming in de Golf van Maine keert 900 jaar afkoeling terug
Snelle opwarming in de Golf van Maine keert 900 jaar afkoeling terug Nieuwe studie toont aan dat microplastics knooppunten worden voor ziekteverwekkers antibiotica-resistente bacteriën
Nieuwe studie toont aan dat microplastics knooppunten worden voor ziekteverwekkers antibiotica-resistente bacteriën Hoe kan een meer zomaar verdwijnen?
Hoe kan een meer zomaar verdwijnen?  Hoe bossen koolstof kunnen terugdringen, ecosystemen kunnen herstellen en banen kunnen creëren
Hoe bossen koolstof kunnen terugdringen, ecosystemen kunnen herstellen en banen kunnen creëren
Hoofdlijnen
- Vleesetende planten inspireren slimme gladde oppervlakken en bionische robots
- Waar en waarom mensen schaatsen maakten van dierlijke botten
- Sterfgevallen chimpansees in Oeganda toegeschreven aan menselijk verkoudheidsvirus
- Veel meer bacteriën hebben elektrisch geleidende filamenten
- Biologen ontdekken de geheimen van hoe genetische eigenschappen worden doorgegeven
- Uw smartphone is mogelijk gelinkt aan krokodillenaanvallen in Indonesië
- Hoe krijgen organismen die seksueel reproduceren hun chromosomen?
- Wat is geheugenverlies precies?
- Het antwoord om elandenpopulaties gezond te houden? Wolven
- Op eieren gebaseerde griepvaccins:niet alles wat ze zijn?

- Nieuwe manier om naar celmembranen te kijken, kan de manier veranderen waarop we ziekten bestuderen
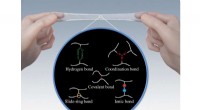
- Elastomeren ontwikkelen sterkere hechtingsbanden
- Betere oplossingen voor het maken van waterstof liggen misschien net aan de oppervlakte

- Cyborg-technologie kan nieuwe diagnostiek mogelijk maken, samensmelting van mens en AI
 Waarom jonge werknemers hun banen op het gebied van fossiele brandstoffen verlaten – en wat u kunt doen als u zin heeft om te stoppen met het klimaat
Waarom jonge werknemers hun banen op het gebied van fossiele brandstoffen verlaten – en wat u kunt doen als u zin heeft om te stoppen met het klimaat  Wat zal geen elektriciteit dragen?
Wat zal geen elektriciteit dragen?  Projectkaarten voor stervorming nabij interstellaire wolken
Projectkaarten voor stervorming nabij interstellaire wolken Wat maakt een hypothese in het wetenschapsexperiment testbaar?
Wat maakt een hypothese in het wetenschapsexperiment testbaar?  Wat is de relatie tussen frequentie en golfsnelheid?
Wat is de relatie tussen frequentie en golfsnelheid?  Heeft leeftijd invloed op de helderheid van sterren?
Heeft leeftijd invloed op de helderheid van sterren?  Hoe dichtbij is te dichtbij? Hydrofracking om toegang te krijgen tot aardgasreservoirs brengt risico's met zich mee voor het oppervlaktewater
Hoe dichtbij is te dichtbij? Hydrofracking om toegang te krijgen tot aardgasreservoirs brengt risico's met zich mee voor het oppervlaktewater  Waarom wordt de mantaal van de aarde beschreven als een semi -vaste stof?
Waarom wordt de mantaal van de aarde beschreven als een semi -vaste stof?
- Elektronica
- Biologie
- Zonsverduistering
- Wiskunde
- French | Italian | Spanish | Portuguese | Swedish | German | Dutch | Danish | Norway |

-
Wetenschap © https://nl.scienceaq.com

