
Wetenschap
Waarom gebruik je ammoniumchloride in plaats van alleen water in de van Grignard -reactie?
Hier is een uitsplitsing:
* Grignard -reagentia zijn zeer reactief: Het zijn sterke bases en nucleofielen, wat betekent dat ze gemakkelijk elektrofielen aanvallen (zoals carbonylverbindingen).
* Water is ook een elektrofiel: Watermoleculen bevatten een gedeeltelijk positief waterstofatoom (vanwege de elektronegativiteit van zuurstof), waardoor ze vatbaar zijn voor aanvallen door Grignard -reagentia.
* ongewenste zijreacties met water: Als water aanwezig is tijdens de Grignard -reactie, zal het Grignard -reagens ermee reageren en een alkaan- en magnesiumhydroxide vormen. Deze reactie verbruikt het Grignard -reagens, vermindert zijn opbrengst en maakt het nutteloos voor de gewenste reactie met de doelelektrofiel.
Ammoniumchloride is een veiliger alternatief:
* zwak zuur: Het is een zwak zuur dat het Grignard -reagens (RMGX) protoneert en een alkaan- en magnesiumchloride vormt.
* Efficiënt blussen: Deze reactie voorkomt effectief het Grignard -reagens om met water of andere ongewenste elektrofiel te reageren.
* neutralisatie: Het neutraliseert ook het sterke basische magnesiumhydroxide gevormd tijdens het blusproces.
Samenvattend: Ammoniumchloride wordt gebruikt om de Grignard -reactie te blussen omdat het een gecontroleerde en efficiënte manier biedt om de reactie te stoppen zonder het Grignard -reagens op te offeren of ongewenste bijproducten te introduceren.
Laat het me weten als je nog andere vragen hebt!
 Wat is een voorbeeld van een gas dat rechtstreeks in vaste stof verandert?
Wat is een voorbeeld van een gas dat rechtstreeks in vaste stof verandert?  Hoe kun je sucrose uit natriumchloride terugwinnen nadat het in water is opgelost?
Hoe kun je sucrose uit natriumchloride terugwinnen nadat het in water is opgelost?  Een sleutel tot calciumsignalering:structuur van de menselijke IP3R type 3 in zijn ligandvrije toestand
Een sleutel tot calciumsignalering:structuur van de menselijke IP3R type 3 in zijn ligandvrije toestand Wat is de naam van polyatomisch ion in verbinding NA2O2?
Wat is de naam van polyatomisch ion in verbinding NA2O2?  Wat is de houdbaarheid van ijzerchloride?
Wat is de houdbaarheid van ijzerchloride?
 Simulaties tonen aan dat magnetisch veld 10 keer sneller kan veranderen dan eerder werd gedacht
Simulaties tonen aan dat magnetisch veld 10 keer sneller kan veranderen dan eerder werd gedacht Welke planten leven in een Canadees gematigd bos?
Welke planten leven in een Canadees gematigd bos?  Geothermische centrale veroorzaakte aardbeving in Zuid-Korea
Geothermische centrale veroorzaakte aardbeving in Zuid-Korea Stad van hoop rijst op van vuilnisbelt in Madagaskar
Stad van hoop rijst op van vuilnisbelt in Madagaskar Tolwegen zijn goed voor het milieu, wetenschappers bevestigen
Tolwegen zijn goed voor het milieu, wetenschappers bevestigen
Hoofdlijnen
- Wat is een monoploïde nummer?
- Wat zijn 2 real-life voorbeelden van hoe bacteriën nuttig kunnen zijn voor mensen?
- Wat is het proces dat genetische diversiteit in populaties mogelijk maakt, is?
- Hoe zijn levende organismen afhankelijk van de SOI die in water leven volledig onafhankelijk van de grond als hulpbron?
- Welke methode zijn biologen van toepassing om organismen te identificeren en te classificeren op basis van hun ontwikkelingsevolutie gedurende miljarden jaren?
- De illegale schildpaddenhandel - waarom wetenschappers geheimen bewaren
- Met behulp van nieuwe technieken doen onderzoekers verrassende ontdekkingen over hoe de hersenen van vliegen reageren op smaak
- Fossiele ontdekking lost het mysterie op over hoe panda's vegetariër werden
- Stadia van de Menselijke Reproductie
- Cementvrij beton verslaat corrosie en geeft fatbergs de flush

- Video:Wat is vlamstralen?

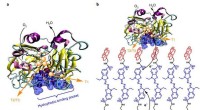
- Verbetering van de elektronenoverdracht in enzymatische biobrandstofcellen
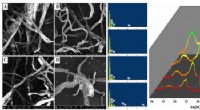
- Wetenschappers rapporteren efficiënt gebruik van oud papier voor de productie van cellulase door Trichoderma longiflorum
- Wetenschappers demonstreren hoe staaleigenschappen kunnen worden verbeterd

 Microben uit vulkanische openingen in de zee onthullen hoe mensen zich aanpasten aan een veranderende atmosfeer
Microben uit vulkanische openingen in de zee onthullen hoe mensen zich aanpasten aan een veranderende atmosfeer Waarom worden sommige mensen honderd? Darmbacteriën kunnen het antwoord bevatten
Waarom worden sommige mensen honderd? Darmbacteriën kunnen het antwoord bevatten  Wat is de gemeenschappelijke eigenschap van jodium en naftaleen?
Wat is de gemeenschappelijke eigenschap van jodium en naftaleen?  Welk metaal roest nooit?
Welk metaal roest nooit?  Hoe Bondorder te berekenen
Hoe Bondorder te berekenen  Wat deden oude Egyptische boeren terwijl de Nijl onder water stond?
Wat deden oude Egyptische boeren terwijl de Nijl onder water stond?  Waarom is water een vloeistof bij kamertemperatuur, terwijl ammoniakgastemperatuur?
Waarom is water een vloeistof bij kamertemperatuur, terwijl ammoniakgastemperatuur?  Het maken van nepvlees roept vragen op over de gezondheid, ethiek en duurzaamheid voor een voormalige slager
Het maken van nepvlees roept vragen op over de gezondheid, ethiek en duurzaamheid voor een voormalige slager
- Elektronica
- Biologie
- Zonsverduistering
- Wiskunde
- French | Italian | Spanish | Portuguese | Swedish | German | Dutch | Danish | Norway |

-
Wetenschap © https://nl.scienceaq.com

