
Wetenschap
Wat is de elektronenstotformule voor molecuul gevormd wanneer waterstof combineert met chloor?
1. Begrijp de valentie -elektronen:
* waterstof (h): Heeft 1 valentie -elektron.
* chloor (CL): Heeft 7 valentie -elektronen.
2. Teken de atomen:
* Schrijf het symbool voor waterstof (H) en chloor (CL) met spaties daartussen.
3. Plaats valentie -elektronen:
* Vertegenwoordig valentie -elektronen als stippen rond de atoomsymbolen.
* Begin stippen afzonderlijk aan de vier zijden van elk atoom te plaatsen.
* Zodra je vier stippen hebt, begin je ze te koppelen.
4. Vorm de binding:
* Waterstof heeft nog een elektron nodig om een stabiele elektronenconfiguratie te bereiken (zoals helium).
* Chloor heeft nog een elektron nodig om een stabiele elektronenconfiguratie te bereiken (zoals argon).
* Ze delen elk één elektron en vormen een enkele covalente binding.
elektronenstipformule voor HCl:
`` `
H • Cl:
:
:
:
`` `
Sleutelpunten:
* Het gedeelde paar elektronen in het midden vertegenwoordigt de enkele covalente binding.
* Zowel waterstof als chloor hebben nu een volledige buitenste schaal van elektronen.
Laat het me weten als je meer voorbeelden wilt zien van elektronenstipformules!
 Hoe sommige insecten erin slagen hun eigen groei te stoppen onder barre omstandigheden
Hoe sommige insecten erin slagen hun eigen groei te stoppen onder barre omstandigheden  Menselijke geografie is de definitie van de menselijke ecologie door wie?
Menselijke geografie is de definitie van de menselijke ecologie door wie?  Een nieuwe methode om de bestuurders van waterdiefstal beter te begrijpen
Een nieuwe methode om de bestuurders van waterdiefstal beter te begrijpen Compostsleutel om koolstof in de bodem vast te leggen
Compostsleutel om koolstof in de bodem vast te leggen Wat is een object gemaakt van ijsstof en rots dat de zon draait?
Wat is een object gemaakt van ijsstof en rots dat de zon draait?
Hoofdlijnen
- Wat gebeurt er tijdens G1 van interfase?
- Zijn planten dieren en schimmels meercellig?
- Wat is een gecultiveerde bron?
- Hoe heet de wetenschap van redeneren?
- Als onderzoekers niet over de eiwitten beschikken die ze nodig hebben, kunnen ze AI ertoe brengen nieuwe structuren te hallucineren
- Theorie hersteld in termen van moderne genetica wordt genoemd?
- Archeologie en ecologie geven samen een vollediger beeld van vroegere relaties tussen mens en natuur
- Waar staat een stand voor in de wetenschap?
- Wat is een verandering of signaal in de omgeving die een organisme kan laten reageren?
- Biochemici duiken in de gezondheidsvoordelen van olijven en olijfolie

- Onderzoekers vinden een manier om slijmerige biofilms zoals oude stickers af te pellen

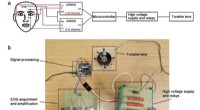
- Ooggestuurde zachte lens maakt de weg vrij voor zachte mens-machine-interfaces
- Chemici ontdekken onverwachte enzymstructuur

- Decennia lang onderzoek mondt uit in een nieuwe manier om links- en rechtshandige moleculen te maken

 Hoe krijgt een raket potentiële energie?
Hoe krijgt een raket potentiële energie?  Hoe veeboeren in Brazilië de CO2-uitstoot kunnen helpen verminderen
Hoe veeboeren in Brazilië de CO2-uitstoot kunnen helpen verminderen  Platina:wat is er zo speciaal aan het glanzende metaal?
Platina:wat is er zo speciaal aan het glanzende metaal?  Hoe eeuwenoude botten uit de historische scheepswrakken van Australië ons kunnen helpen bij het oplossen van misdaden
Hoe eeuwenoude botten uit de historische scheepswrakken van Australië ons kunnen helpen bij het oplossen van misdaden Oppervlaktechemie modelleren en nieuwe materialen voorspellen
Oppervlaktechemie modelleren en nieuwe materialen voorspellen Hoe ontstaat een bergtop?
Hoe ontstaat een bergtop?  Waarom valt de aarde niet gewoon in de zon?
Waarom valt de aarde niet gewoon in de zon?  Wat zal elektrische auto's een boost geven in de VS?
Wat zal elektrische auto's een boost geven in de VS?
- Elektronica
- Biologie
- Zonsverduistering
- Wiskunde
- French | Italian | Spanish | Portuguese | Swedish | German | Dutch | Danish | Norway |

-
Wetenschap © https://nl.scienceaq.com

