
Wetenschap
Wat heeft de kleinste eerste ionisatie -energie carbonsiliconaluminumboron uit deze elementen?
Dit is waarom:
* ionisatie -energie is de energie die nodig is om één elektron uit een atoom in zijn gasvormige toestand te verwijderen.
* factoren die de ionisatie -energie beïnvloeden:
* Nucleaire lading: Een hogere nucleaire lading (meer protonen) trekt elektronen sterker aan, waardoor het moeilijker is om ze te verwijderen (hogere ionisatie -energie).
* Elektronafscherming: Elektronen in binnenschalen schild buitenste elektronen van de kern, waardoor de aantrekkingskracht wordt verminderd.
* Elektronenconfiguratie: Elektronen in hogere energieniveaus zijn verder van de kern en gemakkelijker te verwijderen.
Laten we de elementen analyseren:
* boron (b): Heeft een kleinere atoomradius en een hogere effectieve nucleaire lading in vergelijking met de andere drie elementen. Dit maakt het moeilijker om een elektron te verwijderen.
* koolstof (c): Net als Boron heeft het een relatief hoge ionisatie -energie.
* silicium (si): Grotere atoomradius en iets minder effectieve nucleaire lading dan boor en koolstof.
* aluminium (AL): Grootste atoomstraal uit de vier elementen. Het buitenste elektron in aluminium is verder van de kern en afgeschermd door meer binnenste elektronen. Dit maakt het het gemakkelijkst te verwijderen, wat resulteert in de laagste ionisatie -energie.
Daarom heeft aluminium de kleinste eerste ionisatie -energie.
 Wat zijn enkele voorbeelden van fosformaterialen?
Wat zijn enkele voorbeelden van fosformaterialen?  Power dressing:Elektriciteitsgenererend, rekbaar, zelfherstellende materialen voor wearables
Power dressing:Elektriciteitsgenererend, rekbaar, zelfherstellende materialen voor wearables Het geheim van de beste seizoensgebonden warme chocolademelk? Het zit allemaal in de chemie!
Het geheim van de beste seizoensgebonden warme chocolademelk? Het zit allemaal in de chemie! Is het een goed wetenschappelijk project om pillen met vloeistoffen op te lossen?
Is het een goed wetenschappelijk project om pillen met vloeistoffen op te lossen?  Zijn substraten en reactanten hetzelfde?
Zijn substraten en reactanten hetzelfde?
Hoofdlijnen
- Onderzoek toont aan hoe het dieet van een hond zijn darmmicrobioom vormt
- Welke twee componenten worden in alle wetenschappelijke studies gevonden?
- Endoplasmatisch reticulum:ruw ER versus glad ER
- Uitvindingen in 1947
- Nieuwe methode produceert verser en smakelijker koudgeperst Concord-druivensap
- Wat is de basis van evolutie?
- Van baanbrekend tot baanbrekend:hoe een unieke tomatenmutatie de duurzame landbouw kan transformeren
- Wat is een zeer vertakte opstelling van glucosemoleculen die worden gevonden in lever- en skeletspiercellen?
- Wat moet DNA doen voordat chromosomen kunnen worden gevormd?
- Grootste record voor aromatische ringmaat verbroken met 162 π elektronen
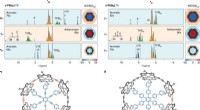
- Gemanipuleerde genetische machinerie afgeleid van E. coli levert nieuwe aminozuren aan eiwitten
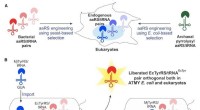
- Wetenschappers ontwerpen nieuwe eiwitstructuur
- Meteorietinslagen kunnen een onverwachte vorm van silica veroorzaken
- Goed verbonden door amiden

 Wat is de rode stip op Jupiter?
Wat is de rode stip op Jupiter?  Afbeelding:De duisternis van de ruimte simuleren
Afbeelding:De duisternis van de ruimte simuleren Wat is de pH van ammoniumfosfaat?
Wat is de pH van ammoniumfosfaat?  Welke voedingsmiddelen zijn macromoleculen?
Welke voedingsmiddelen zijn macromoleculen?  De industrie, en niet de overheid, staat een rechtvaardige transitie voor olie- en gasarbeiders in de weg, zeggen onderzoekers
De industrie, en niet de overheid, staat een rechtvaardige transitie voor olie- en gasarbeiders in de weg, zeggen onderzoekers  Uit onderzoek blijkt dat vrouwen de houding van een man ten opzichte van losse seksuele relaties kunnen voorspellen op basis van zijn gezicht
Uit onderzoek blijkt dat vrouwen de houding van een man ten opzichte van losse seksuele relaties kunnen voorspellen op basis van zijn gezicht Wat is de naam van organel die betrokken is bij zuurstof die proces vereist door welke energie -macromoleculen ATP heeft opgeslagen?
Wat is de naam van organel die betrokken is bij zuurstof die proces vereist door welke energie -macromoleculen ATP heeft opgeslagen?  Succesvolle waarnemingen van de dynamiek van één molecuul met lage röntgendoses
Succesvolle waarnemingen van de dynamiek van één molecuul met lage röntgendoses
- Elektronica
- Biologie
- Zonsverduistering
- Wiskunde
- French | Italian | Spanish | Portuguese | Swedish | German | Dutch | Danish | Norway |

-
Wetenschap © https://nl.scienceaq.com

