
Wetenschap
Welk chloor heeft dezelfde elektronenopstelling als neon?
* neon (ne) is een edelgas met een atoomnummer van 10. Dit betekent dat het 10 protonen en 10 elektronen heeft. De elektronenconfiguratie is 2, 8. Deze opstelling van elektronen is zeer stabiel, daarom zijn edelgassen niet -reactief.
* chloor (Cl) heeft een atoomnummer van 17. Dit betekent dat het 17 protonen en 17 elektronen heeft. De elektronenconfiguratie is 2, 8, 7. De buitenste schaal van chloor (de derde schaal) heeft 7 elektronen, waardoor het minder stabiel is.
Door één elektron te winnen, zal de buitenste schaal van chloor 8 elektronen hebben, net als de buitenste schaal van Neon. Dit geeft chloor dezelfde stabiele elektronenconfiguratie als neon, waardoor het stabieler wordt.
 Onderzoekers versterken zwakste schakel in productie van sterke materialen
Onderzoekers versterken zwakste schakel in productie van sterke materialen Hoe kunnen chemici met zekerheid zeggen dat niemand een element tussen zwavel en chloor zal ontdekken?
Hoe kunnen chemici met zekerheid zeggen dat niemand een element tussen zwavel en chloor zal ontdekken?  Zuren met drie of meer elementen zijn?
Zuren met drie of meer elementen zijn?  Mineralen met de silicium-zuurstofstructuur worden ingedeeld in welke groep?
Mineralen met de silicium-zuurstofstructuur worden ingedeeld in welke groep?  Wat is de relatie tussen structuur van een atoom- en atoomspectra?
Wat is de relatie tussen structuur van een atoom- en atoomspectra?
 Verontrustende omvang van plasticvervuiling onthuld
Verontrustende omvang van plasticvervuiling onthuld Zwarte koolstof van het zuidelijk halfrond volgen naar Antarctische sneeuw
Zwarte koolstof van het zuidelijk halfrond volgen naar Antarctische sneeuw Satelliet ziet tropische cycloon Titli aan land komen in Noordoost-India
Satelliet ziet tropische cycloon Titli aan land komen in Noordoost-India Het verlies van poolijs is zorgwekkend, maar de reus die zich in het zuiden beweegt, kan nog erger zijn
Het verlies van poolijs is zorgwekkend, maar de reus die zich in het zuiden beweegt, kan nog erger zijn Mariene organismen kunnen een plastic zak in 1,75 miljoen stukjes versnipperen, studie toont
Mariene organismen kunnen een plastic zak in 1,75 miljoen stukjes versnipperen, studie toont
Hoofdlijnen
- Wat is het RNA van een plantencel?
- Wat is het belangrijkste enzym dat betrokken is bij de Krebs -cyclus?
- Wat is het kenmerk van een celmembraan dat regelt welke stoffen cel kunnen binnenkomen en verlaten?
- Soorten organismen die van plantencellen zijn gemaakt
- Gliale cellen (Glia): definitie, functie, typen
- Wat een specimencollectie helpt een wetenschapper onderzoek te doen?
- High School Biology Topics
- Wat wij een ASRTONOMICAL -eenheid?
- Droombetekenissen uitgelegd
- Ladingsverandering:hoe elektrische krachten variëren in colloïden

- Natuurlijke stoffen zijn veelbelovend tegen het coronavirus

- Afluisteren van afzonderlijke moleculen met licht door het gebabbel opnieuw af te spelen

- Team gebruikt heet water om fotokatalysator te vormen
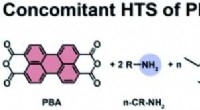
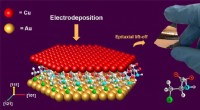
- Onderzoekers gebruiken aminozuren om hoogwaardige dunne koperfilms te laten groeien
 Wie rijdt wie? Klimaat en koolstofcyclus in voortdurende interactie
Wie rijdt wie? Klimaat en koolstofcyclus in voortdurende interactie Wat zijn de secties van DNA die codeert voor een eiwit en de kern verlaten?
Wat zijn de secties van DNA die codeert voor een eiwit en de kern verlaten?  Wat is het plastic als laag gemaakt van soild rock die langzaam stroomt?
Wat is het plastic als laag gemaakt van soild rock die langzaam stroomt?  Hoe infrarood licht kan worden opgevangen door grafeen-nanostructuren
Hoe infrarood licht kan worden opgevangen door grafeen-nanostructuren Vier nieuwe astronauten gaan naar het internationale ruimtestation voor een verblijf van zes maanden
Vier nieuwe astronauten gaan naar het internationale ruimtestation voor een verblijf van zes maanden  Een bal wordt horizontaal vanaf een klif gegooid en raakt 4 seconden later 40 meter aan de voet van de klif de grond. Hoe snel werd gegooid?
Een bal wordt horizontaal vanaf een klif gegooid en raakt 4 seconden later 40 meter aan de voet van de klif de grond. Hoe snel werd gegooid?  Welk type van de vier typen macromoleculen bevatten eenheden die monosacchriden worden genoemd?
Welk type van de vier typen macromoleculen bevatten eenheden die monosacchriden worden genoemd?  Welk type energie heeft een slingerklok?
Welk type energie heeft een slingerklok?
- Elektronica
- Biologie
- Zonsverduistering
- Wiskunde
- French | Italian | Spanish | Portuguese | Swedish | German | Dutch | Danish | Norway |

-
Wetenschap © https://nl.scienceaq.com

