
Wetenschap
Wat is de ionische formule voor barium en fosfaat?
Hier leest u hoe u de ionische formule voor barium en fosfaat kunt bepalen:
* Identificeer de ionen:
* Barium (BA) vormt een +2 ion (ba²⁺).
* Fosfaat (PO₄) vormt een -3 ion (po₄³⁻).
* Breng de kosten in evenwicht: Om een neutrale verbinding te bereiken, moet u het minst gebruikelijke veelvoud van de ladingen vinden. In dit geval is het minst gebruikelijke veelvoud van 2 en 3 6.
* Bepaal de subscripts:
* Om een +6 lading te krijgen, hebt u 3 bariumionen nodig (3 ba²⁺ =+6).
* Om een -6 lading te krijgen, heb je 2 fosfaationen nodig (2 po₄³⁻ =-6).
* Schrijf de formule: De ionische formule voor bariumfosfaat is ba₃ (po₄) ₂ .
 MIT-expert:Hoe milieuverdragen kunnen worden aangescherpt
MIT-expert:Hoe milieuverdragen kunnen worden aangescherpt  De nieuwste duurzaamheidsdoelstellingen van de VN doen meer kwaad dan goed voor het milieu, wetenschappers waarschuwen
De nieuwste duurzaamheidsdoelstellingen van de VN doen meer kwaad dan goed voor het milieu, wetenschappers waarschuwen Digitale ruimte vervangt de openbare ruimte niet, en misschien zelfs helpen om het beter te maken
Digitale ruimte vervangt de openbare ruimte niet, en misschien zelfs helpen om het beter te maken Januari was officieel de warmste maand van Australië ooit
Januari was officieel de warmste maand van Australië ooit Wat is klimaat?
Wat is klimaat?
Hoofdlijnen
- Onthul de geheimen van plantgezondheid en koolstofopslag met rhizosphere-on-a-chip
- Hoe produceren wetenschappers een wetenschappelijke theorie?
- Inzicht in de manier waarop bruinrotschimmels hout afbreken, zou kunnen leiden tot nieuwe hulpmiddelen voor een efficiëntere productie van biobrandstoffen
- Wat heeft Virchow bijgedragen aan de celtheorie?
- Acute tastzin helpt kolibries dichtbij een bloem te zweven zonder er tegenaan te botsen, blijkt uit onderzoek
- Wat is de functie van slijm in zowel de luchtwegen als het maagdarmkanaal?
- Wat voor soort enzym breekt koolhydraten af?
- Hoe pathogene bacteriën de slingers en pijlen van infectie doorstaan
- Oorlog tegen haaien:hoe malafide vissersvloten het grootste roofdier van de oceaan plunderen
- Flow chemie techniek biedt snellere, veiligere manier om te screenen, bestuderen en optimaliseren van industriële chemische reacties

- Gebruik van glaskeramiek in kaslampen faciliteert plantengroei

- De geheimen achter een griezelige fotografische techniek

- Brandstof en chemicaliën uit plantaardig afval

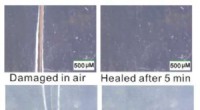
- Wetenschappers ontdekken nieuw type zelfherstellend materiaal
 Wat is het aantal atomen in Ca(NO3)2?
Wat is het aantal atomen in Ca(NO3)2?  Onderzoekers demonstreren recordsnelheid met geavanceerde spectroscopietechniek
Onderzoekers demonstreren recordsnelheid met geavanceerde spectroscopietechniek Zeldzame gletsjeronderzoeksnotitieboekjes nu digitaal verkrijgbaar
Zeldzame gletsjeronderzoeksnotitieboekjes nu digitaal verkrijgbaar Wat is een korte termijn voor energiebron?
Wat is een korte termijn voor energiebron?  Wat zijn woestijngronden en bergbodems?
Wat zijn woestijngronden en bergbodems?  Waarom zou een bergachtig gebied met overvloedige regenval meestal meer rotsval hebben dan berg in een droog klimaat?
Waarom zou een bergachtig gebied met overvloedige regenval meestal meer rotsval hebben dan berg in een droog klimaat?  Hoe heeft de wetenschap zijn naam gekregen?
Hoe heeft de wetenschap zijn naam gekregen?  Palmolie:de koolstofkosten van ontbossing
Palmolie:de koolstofkosten van ontbossing
- Elektronica
- Biologie
- Zonsverduistering
- Wiskunde
- French | Italian | Spanish | Portuguese | Swedish | German | Dutch | Danish | Norway |

-
Wetenschap © https://nl.scienceaq.com

