
Wetenschap
Welke twee atomen zouden meestal voor een covalente binding?
Dit is waarom:
* niet -metalen Heb een hoge elektronegativiteit, wat betekent dat ze een sterke aantrekkingskracht hebben op elektronen.
* In een covalente binding delen atomen elektronen om een stabiele elektronenconfiguratie te bereiken (zoals een edelgas).
* Aangezien beide niet -metalen een sterke trek van elektronen hebben, delen ze eerder dan het ene atoom dat een elektron volledig van het andere neemt (dat een ionische binding zou vormen).
Voorbeelden van atomen die gewoonlijk covalente bindingen vormen:
* waterstof (h)
* koolstof (c)
* zuurstof (O)
* stikstof (n)
* fluor (f)
* chloor (Cl)
* bromine (br)
* jodium (i)
Opmerking: Er zijn enkele uitzonderingen op deze regel. Een metaalachtige boor kan bijvoorbeeld soms covalente bindingen vormen.
Hoofdlijnen
- Waar vindt osmose plaats in het spijsverteringsstelsel?
- Waar worden vezels gefermenteerd in het spijsverteringskanaal van het varken?
- Nieuwe coronavirusvariant:wat is het spike-eiwit en waarom zijn mutaties erop belangrijk?
- Hoe wordt een wetenschappelijke hypothese gevormd?
- Wat is een structuur in de kern waar RNA is getranscribeerd?
- Nieuw genomisch onderzoek biedt een glimp van hoe walvissen zich kunnen aanpassen aan de oceaan
- Zorg voor honden met speciale behoeften
- Vonnis voor natuurmysterie in Nevada, waar uit DNA-tests blijkt dat wolven coyotes waren
- Welk type lipide is het belangrijkst in celmembranen?
- Onderzoek onthult hoe een klein molecuul de verwijdering van overtollig cholesterol bevordert
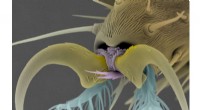
- Goedkoop, fly footpad-achtige zelfklevende structuur die herhaaldelijk kan worden bevestigd/losgemaakt
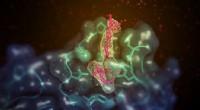
- Wetenschappers gebruiken chemische hulpmiddelen om kankerverwekkende eiwitten op te sporen

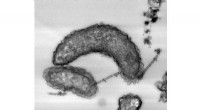
- IJzercorroderende bacteriën blijken enzymen te bezitten waardoor ze elektronen uit extracellulaire vaste stoffen kunnen halen
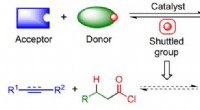
- Voorlopers van zuurchloride maken met behulp van shuttle-katalyse
 Wat is de korsttemperatuur?
Wat is de korsttemperatuur?  Waar komen poolmuggen het meest voor in Groenland en waarom?
Waar komen poolmuggen het meest voor in Groenland en waarom?  Wat zijn feiten over de omgeving?
Wat zijn feiten over de omgeving?  Als u alle energie die gerelateerd is aan beweging gemeten en in deeltjes van een stof wordt opgeslagen, wat zou er meten?
Als u alle energie die gerelateerd is aan beweging gemeten en in deeltjes van een stof wordt opgeslagen, wat zou er meten?  Met unieke gegevens, onderzoekers volgen het effect van het Braziliaanse sojamoratorium op een oprukkende landbouwgrens
Met unieke gegevens, onderzoekers volgen het effect van het Braziliaanse sojamoratorium op een oprukkende landbouwgrens Efficiënter, duurzamere vaste oxide brandstofcellen
Efficiënter, duurzamere vaste oxide brandstofcellen Welke minder energie is een golf, hoe kleiner het?
Welke minder energie is een golf, hoe kleiner het?  Hoe worden de gameten geproduceerd door Meiosis?
Hoe worden de gameten geproduceerd door Meiosis?
- Elektronica
- Biologie
- Zonsverduistering
- Wiskunde
- French | Italian | Spanish | Portuguese | Swedish | German | Dutch | Danish | Norway |

-
Wetenschap © https://nl.scienceaq.com


