
Wetenschap
Vormen fluor en chloor een ionische binding?
* elektronegativiteit: Zowel fluor als chloor zijn zeer elektronegatieve elementen. Dit betekent dat ze een sterke neiging hebben om elektronen aan te trekken.
* Vergelijkbare elektronegativiteit: Hoewel fluor het meest elektronegatieve element is, is chloor ook zeer elektronegatief. Hun elektronegativiteitsverschil is niet groot genoeg om een volledige overdracht van elektronen te veroorzaken, wat nodig is voor een ionische binding.
* Covalente binding: Vanwege hun vergelijkbare elektronegativiteit zullen fluor en chloor elektronen delen om een covalente binding te vormen. Dit komt omdat geen van beide atoom een sterk genoeg trek heeft om een elektron van de andere volledig te nemen.
Samenvattend: Het elektronegativiteitsverschil tussen fluor en chloor is niet significant genoeg om een ionische binding te vormen. In plaats daarvan delen ze elektronen om een covalente binding te vormen.
 Onderzoekers creëren methode die infecties snel en nauwkeurig kan detecteren
Onderzoekers creëren methode die infecties snel en nauwkeurig kan detecteren Hoeveel elektronen zijn er in het buitenste energieniveau van een chloride-ionen (Cl-) tafelzout?
Hoeveel elektronen zijn er in het buitenste energieniveau van een chloride-ionen (Cl-) tafelzout?  Het aantal atomen in een monster berekenen
Het aantal atomen in een monster berekenen Geven zure oplossingen enkele of veel waterstofionen?
Geven zure oplossingen enkele of veel waterstofionen?  Warmtegeleidingsproeven voor kinderen
Warmtegeleidingsproeven voor kinderen
 De door hitte vastgehouden kooldioxide- en methaanniveaus in de lucht bereikten vorig jaar opnieuw recordhoogten
De door hitte vastgehouden kooldioxide- en methaanniveaus in de lucht bereikten vorig jaar opnieuw recordhoogten  Natte winter maakt geen einde aan risico op klimaatverandering voor Colorado River
Natte winter maakt geen einde aan risico op klimaatverandering voor Colorado River Zonlicht breekt polystyreen sneller af dan verwacht
Zonlicht breekt polystyreen sneller af dan verwacht Wat was het tweede organisme dat op aarde verscheen?
Wat was het tweede organisme dat op aarde verscheen?  Een presentatie starten op Fast Food
Een presentatie starten op Fast Food
Hoofdlijnen
- Hoe superbacteriën spiegelbeelden gebruiken om antibioticaresistentie te creëren
- Welk RNA is het gevolg van transcriptie?
- Wat voor soort plant wordt rottende groenten gemaakt?
- Hoe is de bevruchting anders dan de ontwikkeling van het embryo?
- Wat is het doel van de vrucht die zich ontwikkelt op een bloeiende plant?
- Wat is een bijestinfectie?
- Beschrijf de relatie tussen DNA en eiwitten?
- Aziatische bossen tonen veerkracht ondanks toenemende verstoringen als gevolg van klimaatverandering en menselijke activiteiten
- Wanneer ontwikkelen baby's liefde voor spraak?
- Hoe kooldioxide uit de lucht te zuigen voor brandstoffen en meer?

- Onderzoekers stemmen de kleur en thermische eigenschappen van materialen afzonderlijk af

- Leren van mosselen:een tweekleppige zeedier inspireert onderzoekers om sterkere polymeren te maken

- Botdiep:Mineraal gevonden in menselijk bot kan helpen bij het bestrijden van giftige organische stoffen
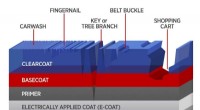
- Om autocoatings te verbeteren, nieuwe tests doen meer dan krassen op het oppervlak
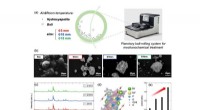
 Zeer lichtgevende inkten gemaakt van koper-jodium hybride clusters met aggregatie-geïnduceerde emissie
Zeer lichtgevende inkten gemaakt van koper-jodium hybride clusters met aggregatie-geïnduceerde emissie Welke energietransformatie vindt plaats in een gasoven?
Welke energietransformatie vindt plaats in een gasoven?  Fermilab bereikt veld van 14,5 tesla voor versnellermagneet, nieuw wereldrecord neerzetten
Fermilab bereikt veld van 14,5 tesla voor versnellermagneet, nieuw wereldrecord neerzetten Vroege adolescentie centraal in genderongelijkheid in Azië-Pacific
Vroege adolescentie centraal in genderongelijkheid in Azië-Pacific Wat zijn de instrumenten die worden gebruikt in windenergie?
Wat zijn de instrumenten die worden gebruikt in windenergie?  Welke planeet in uw zonnestelsel heeft het meest gewelddadige weer?
Welke planeet in uw zonnestelsel heeft het meest gewelddadige weer?  Wanneer is de eenvoudige lichtmicroscoop uitgevonden?
Wanneer is de eenvoudige lichtmicroscoop uitgevonden?  Bio-geïnspireerd proces maakt materialen licht, robuust, programmeerbaar op nano- tot macroschaal
Bio-geïnspireerd proces maakt materialen licht, robuust, programmeerbaar op nano- tot macroschaal
- Elektronica
- Biologie
- Zonsverduistering
- Wiskunde
- French | Italian | Spanish | Portuguese | Swedish | German | Dutch | Danish | Norway |

-
Wetenschap © https://nl.scienceaq.com

