
Wetenschap
Wat is het kookpunt van een 2,47 molaal oplossing napthaleen in Benzenethe benzeen 80.1?
Inzicht in de concepten
* molaliteit (m): Molaliteit is het aantal mol opgeloste stof per kilogram oplosmiddel.
* Kookpunthoogte: Wanneer een niet-vluchtige opgeloste stof (zoals naftaleen) wordt opgelost in een oplosmiddel (zoals benzeen), neemt het kookpunt van de oplossing toe. Dit staat bekend als kookpunthoogte.
* Kookpunthoogteconstante (KB): Deze constante is specifiek voor het oplosmiddel en vertegenwoordigt de verandering in kookpunt per molale opgeloste concentratie. Voor benzeen, Kb =2,53 ° C/m.
het berekenen van het kookpunthoogte
1. Gebruik de formule: Δtb =kb * m
* Δtb =verandering in kookpunt
* Kb =kookpunthoogteconstante (2,53 ° C/m voor benzeen)
* m =molaliteit (2,47 m)
2. Sluit de waarden aan: Δtb =(2,53 ° C/m) * (2,47 m) =6,25 ° C
het berekenen van het uiteindelijke kookpunt
1. Voeg het kookpunthoogte toe aan het normale kookpunt van benzeen:
* Laatste kookpunt =normaal kookpunt van benzeen + Δtb
* Laatste kookpunt =80,1 ° C + 6,25 ° C =86,35 ° C
Daarom is het kookpunt van een 2.47 molale oplossing van naftaleen in benzeen ongeveer 86,35 ° C.
 Nieuw basalttype ontdekt onder de oceaan
Nieuw basalttype ontdekt onder de oceaan Op welke landen en continenten kunt u het bladverliezende bosbioom vinden?
Op welke landen en continenten kunt u het bladverliezende bosbioom vinden?  Rina nu een grote post-tropische storm in de noordelijke centrale Atlantische Oceaan
Rina nu een grote post-tropische storm in de noordelijke centrale Atlantische Oceaan De antropogene toename van koolstofdioxide op aarde is ongekend
De antropogene toename van koolstofdioxide op aarde is ongekend Duizenden vissen zijn dood aangetroffen in Biscayne Bay. Koraalverbleking is misschien de volgende
Duizenden vissen zijn dood aangetroffen in Biscayne Bay. Koraalverbleking is misschien de volgende
Hoofdlijnen
- Zeeslakken weten hoe ze hun huisvestingskosten moeten begroten
- Welk idee zegt dat een soort organisme beter in staat is om in zijn omgeving te overleven dan een ander zal meer nakomelingen produceren en overheersend worden?
- Waarom is het classificatiesysteem belangrijk voor wetenschappers?
- Onderzoekers vinden pesticiden in een derde van de geteste Australische kikkers. Hebben deze massale sterfgevallen veroorzaakt?
- Wat zijn de 3 meest voorkomende elementen in menselijke lichamen?
- Zeldzame diepzee-inktvis gefilmd op diepte
- Wat is de relatie tussen fysieke en biologische wetenschap?
- Wanneer een blaasje combineert met het celmembraan om van deeltjes af te komen, wat gebeurt er?
- Het menselijk genoomproject heeft de sequentie van basenparen in zijn geheel bepaald. Hoe heeft dit een directe invloed op ons begrip van genetische ziekten?
- Kleine bruggen helpen deeltjes aan elkaar te plakken

- Onderzoekers vinden potentiële nieuwe bron van zeldzame aardelementen

- Additieve fabricage van multifunctionele onderdelen

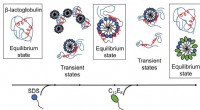
- Met zeep betrapt:begrijpen hoe zeepmoleculen eiwitten helpen om in en uit vorm te komen
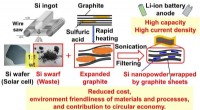
- Van afval tot schat:Siliciumafval vindt een nieuwe toepassing in Li-ionbatterijen
 Nieuwe techniek kan gevangen koolstof waardevoller maken
Nieuwe techniek kan gevangen koolstof waardevoller maken Als u alle gerelateerde beweging en opgeslagen energie in deeltjes van een stof gemeten zou zijn?
Als u alle gerelateerde beweging en opgeslagen energie in deeltjes van een stof gemeten zou zijn?  Onderzoek naar de botsing van mannelijke identiteiten op een internethaatsite
Onderzoek naar de botsing van mannelijke identiteiten op een internethaatsite  Kristallen die aan boord van het ruimtestation zijn gekweekt, bieden technologie voor het detecteren van straling
Kristallen die aan boord van het ruimtestation zijn gekweekt, bieden technologie voor het detecteren van straling Hoe bereken ik minuten in een fractie van een uur?
Hoe bereken ik minuten in een fractie van een uur?  Vormen geïsoleerde atomen spontaan gevormd?
Vormen geïsoleerde atomen spontaan gevormd?  Oekraïne opent gigantische koepel boven verwoeste reactor van Tsjernobyl
Oekraïne opent gigantische koepel boven verwoeste reactor van Tsjernobyl Wat gebeurt er als Mercurius de aarde en de zon passeert?
Wat gebeurt er als Mercurius de aarde en de zon passeert?
- Elektronica
- Biologie
- Zonsverduistering
- Wiskunde
- French | Italian | Spanish | Portuguese | Swedish | German | Dutch | Danish | Norway |

-
Wetenschap © https://nl.scienceaq.com

