
Wetenschap
Bij standaarddruk heeft een bepaalde verbinding een laag kookpunt en is het onoplosbaar in water STP dit waarschijnlijk bestaat als?
* Laag kookpunt: Dit suggereert zwakke intermoleculaire krachten tussen de moleculen van de verbinding.
* onoplosbaar in water: Dit houdt in dat de verbinding niet-polair is of zeer zwakke interacties heeft met watermoleculen. Water is een polair oplosmiddel, dus het levert de voorkeur aan andere polaire moleculen op te lossen.
* Standaarddruk (STP): Dit vertelt ons alleen maar de voorwaarden waar we onder werken, maar het heeft geen direct invloed op het type verbinding.
het samenstellen:
Gezien de aanwijzingen is de verbinding hoogstwaarschijnlijk een niet-polair covalente molecuul. Dit is waarom:
* Zwakke intermoleculaire krachten: Niet-polaire moleculen ervaren voornamelijk zwakke dispersiekrachten in Londen, die verantwoordelijk zijn voor hun lage kookpunten.
* Insolubheid in water: De regel "Like Lost Like" -regel is hier van toepassing. Water is polair en niet-polaire moleculen worden er niet door aangetrokken, wat leidt tot onoplosbaarheid.
Voorbeelden van dergelijke verbindingen kunnen zijn:
* Kleine koolwaterstoffen: Zoals methaan (CH4) en ethaan (C2H6)
* gassen: Veel gassen bestaan als niet-polaire moleculen bij standaarddruk (bijv. Stikstof (N2), zuurstof (O2))
Belangrijke opmerking: Er zijn uitzonderingen. Hoewel veel niet-polaire moleculen deze eigenschappen vertonen, kunnen sommige verbindingen andere factoren hebben die hun gedrag beïnvloeden. Een groot molecuul met een niet-polaire ruggengraat kan bijvoorbeeld nog steeds enkele polaire functionele groepen hebben die kunnen leiden tot zwakke oplosbaarheid in water.
 Ontbossing gekoppeld aan palmolieproductie maakt Indonesië warmer
Ontbossing gekoppeld aan palmolieproductie maakt Indonesië warmer Parijs, Tokio, New York en anderen beloven afval te verminderen
Parijs, Tokio, New York en anderen beloven afval te verminderen Biologische gevolgen van klimaatverandering voor epidemieën kunnen schaalafhankelijk zijn
Biologische gevolgen van klimaatverandering voor epidemieën kunnen schaalafhankelijk zijn Hoe maak je een Shoebox Biome voor school
Hoe maak je een Shoebox Biome voor school  Wat zijn de belangrijkste dingen die het universum vormen?
Wat zijn de belangrijkste dingen die het universum vormen?
Hoofdlijnen
- Hoe ons album met opnames van vogelgezang naar #2 in de ARIA-hitlijsten schoot
- Wetenschappers ontdekken dat schorpioenen zich richten op hun gif
- Seks:waarom moeite doen? Wetenschappers onderzoeken evolutionaire mysteries
- Wat gebeurt er met het nucleolus en nucleair membraan tijdens celdeling?
- Wat is homeostaris?
- Octopussen geven de voorkeur aan bepaalde wapens bij het jagen en passen tactieken aan hun prooi aan
- Kenmerken van een eencellig organisme
- Wat zijn de twee belangrijkste functies van nucleïnezuur in levende wezens?
Nucleïnezuren zijn kleine stukjes materie met grote rollen om te spelen. Genoemd naar hun locatie - de kern - deze zuren dragen informatie die cellen helpt bij het maken va
- Waar kan de stengel van een plant voor worden gebruikt?
- Lab-on-a-chip-test heeft potentieel om COVID-19-immuunrespons sneller te detecteren dan huidige antilichaamtesten

- Aangeraakt door licht:Foto-geëxciteerde stannylanionen zijn geweldig voor het produceren van organotinverbindingen

- Video:Waarom ruiken de poten van mijn hond naar Fritos?

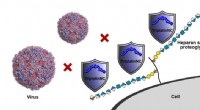
- Op metaal gebaseerde verbindingen maken de weg vrij voor nieuwe antivirale behandelingen
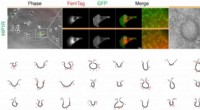
- Nieuwe methode ontdekt om eiwitten in menselijke cellen te bekijken
 Bereken de entropie van verdamping per mol ethanol gegeven enthalpie-verandering is 109,8 JK-1 mol-1 en kookpunt 78.50c?
Bereken de entropie van verdamping per mol ethanol gegeven enthalpie-verandering is 109,8 JK-1 mol-1 en kookpunt 78.50c?  Hoe kan de zon voedsel verwarmen?
Hoe kan de zon voedsel verwarmen?  Wat is het antwoord van traagheid?
Wat is het antwoord van traagheid?  Wat zijn de bouwstenen van suiker?
Wat zijn de bouwstenen van suiker?  Hoe ziet een geel voorwerp eruit als het onder licht staat?
Hoe ziet een geel voorwerp eruit als het onder licht staat?  Hoe wordt het geroepen om omhoog te gaan door smalle buizen tegen de zwaartekracht?
Hoe wordt het geroepen om omhoog te gaan door smalle buizen tegen de zwaartekracht?  Wat zijn alle organismen in een ecosysteem?
Wat zijn alle organismen in een ecosysteem?  Een fysieke hoeveelheid die wordt beschreven door zowel de grootte als de richting wordt genoemd?
Een fysieke hoeveelheid die wordt beschreven door zowel de grootte als de richting wordt genoemd?
- Elektronica
- Biologie
- Zonsverduistering
- Wiskunde
- French | Italian | Spanish | Portuguese | Swedish | German | Dutch | Danish | Norway |

-
Wetenschap © https://nl.scienceaq.com

