
Wetenschap
Hoeveel gram RM NH 3 kan worden geproduceerd uit 2,90 mol N 2?
1. Evenwichtige chemische vergelijking:
De evenwichtige chemische vergelijking voor de reactie van stikstofgas (N₂) met waterstofgas (H₂) om ammoniak (NH₃) te produceren, is:
N₂ + 3H₂ → 2NH₃
2. Mol -verhouding:
Uit de evenwichtige vergelijking zien we dat 1 mol N₂ 2 mol NH₃ produceert.
3. Berekening:
* We hebben 2,90 mol N₂.
* Met behulp van de molverhouding kunnen we de mol NH₃ geproduceerd vinden:2,90 mol N₂ * (2 mol NH₃ / 1 mol N₂) =5,80 mol NH₃
4. Converteer mollen naar gram:
* De molaire massa van NH₃ is 17,03 g/mol (14,01 g/mol voor n + 3 * 1.01 g/mol voor h)
* Vermenigvuldig de mol NH₃ met zijn molaire massa om de massa in gram te krijgen:5.80 mol NH₃ * 17.03 g/mol = 98,7 g NH₃
Daarom kan 98,7 gram NH₃ worden geproduceerd vanaf 2,90 mol N₂.
Hoofdlijnen
- Hoe DNA -pakket zelf?
- Hoe het Human Microbiome-project werkt
- Wat is het metabolisme van zeesterren?
- Kunstmatige selectie (selectieve fokkerij): definitie & voorbeelden
- Welk effect heeft de temperatuur op cellulaire enzymactiviteit?
- Hoe meer leren over massale nesten kan helpen bij het behoud van zeeschildpadden
- Welk deel van het DNA -molecuul bevat genetische informatie die wordt gebruikt om eiwitten te maken?
- Kan JWST het verschil zien tussen een exoEarth en exoVenus?
- Hoe worden restrictie-enzymen gebruikt?
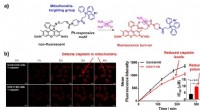
- Een mitochondria-gerichte fluorescerende sonde voor cisplatine
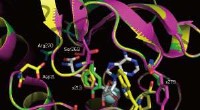
- Gerichte evolutie om enzymen te ontwerpen die beeldvormende middelen maken voor medische diagnose
- Nanogestructureerde materialen op siloxaanbasis voor nieuwe kunststoffen en micro-elektronica

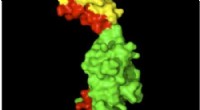
- Nieuw onderzoeksgebied:Hoe eiwitstructuren veranderen door normaalkrachten
- Ontwikkelen van duurzame membranen voor toekomstige energie

 NASA ziet tropische cycloon Joaninha Mauritius treffen
NASA ziet tropische cycloon Joaninha Mauritius treffen Samenwerking levert veelbelovend materiaal op voor quantum computing
Samenwerking levert veelbelovend materiaal op voor quantum computing Onderzoekers gebruiken kunstmatige intelligentie om te identificeren, Graaf, beschrijf wilde dieren
Onderzoekers gebruiken kunstmatige intelligentie om te identificeren, Graaf, beschrijf wilde dieren Hoe vind je een elektron in neutraal atoom?
Hoe vind je een elektron in neutraal atoom?  Hoe de Bungle Bungles aan hun strepen kwamen
Hoe de Bungle Bungles aan hun strepen kwamen Waar vangen planten energie vast en maken ze complexe moleculen?
Waar vangen planten energie vast en maken ze complexe moleculen?  Hoe individuen beslissen tussen eigenbelang en toewijding aan een groep
Hoe individuen beslissen tussen eigenbelang en toewijding aan een groep Hoeveel fotonen zijn er in een uitbarsting van geel licht op 589 nm van de natriumlamp die 609 kJ energie bevat?
Hoeveel fotonen zijn er in een uitbarsting van geel licht op 589 nm van de natriumlamp die 609 kJ energie bevat?
- Elektronica
- Biologie
- Zonsverduistering
- Wiskunde
- French | Italian | Spanish | Portuguese | Swedish | German | Dutch | Danish | Norway |

-
Wetenschap © https://nl.scienceaq.com


