
Wetenschap
In tegenstelling tot natrium en chloor worden sommige atomen stabieler door elektronen te delen wat vormt?
Dit is waarom:
* ionische bindingen: Natrium (NA) heeft één valentie -elektron, terwijl chloor (CL) er zeven heeft. Natrium geeft gemakkelijk zijn elektron op om een positief geladen ion (Na+) te worden, en chloor krijgt gemakkelijk een elektron om een negatief geladen ion te worden (Cl-). Deze tegengestelde ladingen trekken aan en vormen een stabiele ionische binding.
* Covalente bindingen: Atomen zoals zuurstof (O), koolstof (C) en waterstof (H) hebben een sterke neiging om hun valentie -elektronen te delen met andere atomen om een stabiele elektronenconfiguratie te bereiken. Dit delen resulteert in een covalente binding, waarbij twee atomen een of meer paar elektronen delen. Dit gedeelde elektronenpaar wordt aangetrokken tot de kernen van beide atomen en houdt ze bij elkaar.
Voorbeelden van covalente bindingen:
* water (h₂o): Twee waterstofatomen delen hun elektronen met een zuurstofatoom, wat resulteert in twee covalente bindingen.
* methaan (ch₄): Eén koolstofatoom deelt zijn vier elektronen met vier waterstofatomen en vormt vier covalente bindingen.
Key Takeaway: Covalente binding is een sleutelconcept in de chemie en is verantwoordelijk voor de vorming van een breed scala aan moleculen, waaronder die waaronder levende organismen.
Hoofdlijnen
- Verwarde walvis blokkeert de jachthaven van Marseille
- Wat zijn biotische gevaren?
- Welke subtypes van Yersinia zijn verantwoordelijk voor yersinose?
- Wat veroorzaakt brokkelige weefsels?
- Wat voor soort spieren zijn langwerpig gerangschikt in vellen en bevatten meerdere kernen?
- Waterige substantie die het interieur van cellen vult en organellen ophangt?
- Hoe slim te zijn:top 5 manieren om slimmer te worden
- Wat is het kopiëren van de code en heeft dit betrekking op DNA?
- Waarom katten meer levens hebben dan honden als het om slangenbeten gaat
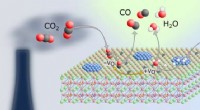
- Nieuwe katalysator voor lagere CO2-uitstoot
- Gezondere zuivelproducten met bacteriële films en nanovezelmembranen

- zachter, veiligere haarverf op basis van synthetische melanine

- Chemici produceren en testen nieuwe elektrolysecel voor vaste oxiden

- Bitterreceptor betrokken bij ontstekingsremmend effect van resveratrol?

 Team ontwikkelt snelle SARS-CoV-2-test op basis van nieuwe plasmonische fluor-biolabelingstechnologie
Team ontwikkelt snelle SARS-CoV-2-test op basis van nieuwe plasmonische fluor-biolabelingstechnologie Welke soorten chemicaliën kunnen worden gebruikt om lipiden op te lossen?
Welke soorten chemicaliën kunnen worden gebruikt om lipiden op te lossen?  Nieuw onderzoek wijst op de impact van de digitale kloof
Nieuw onderzoek wijst op de impact van de digitale kloof Luchtvaartmaatschappijen en passagiers besparen miljarden door crewplanning
Luchtvaartmaatschappijen en passagiers besparen miljarden door crewplanning Wat zijn de namen van eerste 3 planeten in het zonnestelsel "?
Wat zijn de namen van eerste 3 planeten in het zonnestelsel "?  Zwaartekrachtgolfinzichten van internetstralende ballonnen
Zwaartekrachtgolfinzichten van internetstralende ballonnen Ongecontroleerde raketafdalingen vormen een risico van 10% op het doden van een of meer mensen in de komende tien jaar
Ongecontroleerde raketafdalingen vormen een risico van 10% op het doden van een of meer mensen in de komende tien jaar Een heropleving van het virus kan het ontluikende economische herstel ontsporen
Een heropleving van het virus kan het ontluikende economische herstel ontsporen
- Elektronica
- Biologie
- Zonsverduistering
- Wiskunde
- French | Italian | Spanish | Portuguese | Swedish | German | Dutch | Danish | Norway |

-
Wetenschap © https://nl.scienceaq.com


