
Wetenschap
Hoe kan een atoom meer dan één covalente binding vormen?
* valentie -elektronen: Atomen hebben elektronen in hun buitenste schaal genaamd valentie -elektronen. Deze elektronen zijn betrokken bij chemische binding.
* octetregel: Atomen hebben de neiging om elektronen te winnen, verliezen of delen om een stabiele configuratie te bereiken met acht valentie -elektronen (behalve voor waterstof en helium, die er twee nodig hebben). Dit staat bekend als de Octet -regel.
* Meerdere bindingen: Om de octetregel te vervullen, kunnen sommige atomen meer dan één paar elektronen delen met andere atomen. Dit creëert meerdere covalente bindingen:
* Dubbele binding: Twee paar elektronen worden gedeeld (weergegeven door twee lijnen in een Lewis -structuur).
* Triple Bond: Drie paren elektronen worden gedeeld (weergegeven door drie lijnen in een Lewis -structuur).
Voorbeeld:
* koolstof (c): Koolstof heeft vier valentie -elektronen. Om een stabiel octet te bereiken, kan het vier enkele covalente bindingen vormen (zoals in methaan, CH4). Het kan ook dubbele bindingen vormen (zoals in ethyleen, C2H4) of drievoudige bindingen (zoals bij acetyleen, C2H2).
factoren die het aantal covalente bindingen beïnvloeden:
* Aantal valentie -elektronen: Hoe meer valentie -elektronen een atoom heeft, hoe meer bindingen het mogelijk kan vormen.
* elektronegativiteit: De elektronegativiteit van een atoom (zijn vermogen om elektronen aan te trekken) kan het type binding beïnvloeden dat het vormt.
* Atomaire maat: Kleinere atomen hebben de neiging om meer bindingen te vormen vanwege de dichter nabijheid van hun valentie -elektronen.
Samenvattend: Atomen kunnen meerdere covalente bindingen vormen door meerdere paren elektronen te delen om een stabiele elektronenconfiguratie te bereiken en aan de Octet -regel te voldoen.
 Welk gas zijn de reactanten in chemische reactant van fotosynthese?
Welk gas zijn de reactanten in chemische reactant van fotosynthese?  Wat is de chemische naam voor 25 NACI?
Wat is de chemische naam voor 25 NACI?  Wat zijn de juiste omstandigheden voor de autoclaaf?
Wat zijn de juiste omstandigheden voor de autoclaaf?  Ontwikkeling van lithium-luchtbatterijen met ultrahoge capaciteit met behulp van CNT-blad-luchtelektroden
Ontwikkeling van lithium-luchtbatterijen met ultrahoge capaciteit met behulp van CNT-blad-luchtelektroden Kan onthard water een koperen pijp doen corroderen?
Kan onthard water een koperen pijp doen corroderen?
 Gedragsaanpassingen van Aziatische olifanten
Gedragsaanpassingen van Aziatische olifanten  De zaak van de ontbrekende diamanten
De zaak van de ontbrekende diamanten Het verminderen van vervuiling door het wegvervoer kan planten helpen groeien
Het verminderen van vervuiling door het wegvervoer kan planten helpen groeien Verschuiving naar planetair gezondheidsdieet zou van invloed zijn op het Britse landgebruik en de wereldwijde watervoorraden
Verschuiving naar planetair gezondheidsdieet zou van invloed zijn op het Britse landgebruik en de wereldwijde watervoorraden Welke dierenspecifieke leeft in het Amizon -regenwoud?
Welke dierenspecifieke leeft in het Amizon -regenwoud?
Hoofdlijnen
- Wat doet de gladde ER in een dierencel?
- Hoe moet Uber worden gereguleerd?
- Hoe planten 'slechte' moleculen benutten voor goede doeleinden
- 5 manieren waarop je hersenen je emoties beïnvloeden
- Welke organel in een plant laat glucose uit zonlicht komen?
- Wanneer verschenen mannen en vrouwen in de evolutie?
- Wetenschappers winnen de World Food Prize voor hun werk aan de Global Seed Vault
- Gered Irrawaddy dolfijnkalf sterft ondanks wekenlange zorg
- Welke term beschrijft binnenvallende bacterievirussen en parasieten?
- Combinatie van microbiële en chemische vingerafdrukken voor forensische toepassingen

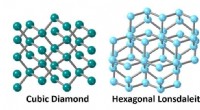
- We hebben in minuten zonder hitte diamanten gemaakt door de kracht van een asteroïdebotsing na te bootsen
- Nieuwe 3D-printtechniek produceert levende 4D-materialen

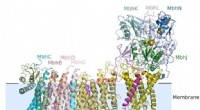
- Microben uit vulkanische openingen in de zee onthullen hoe mensen zich aanpasten aan een veranderende atmosfeer
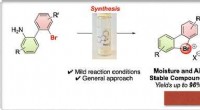
- Cyclische hypervalente brooms werken als aryneprecursoren
 Hoeveel mol natriumsulfaat zijn aanwezig in 0,1000 gram de verbinding?
Hoeveel mol natriumsulfaat zijn aanwezig in 0,1000 gram de verbinding?  Uit simulaties blijkt dat delen van Amazon in 2050 van koolstofput naar bron kunnen overschakelen
Uit simulaties blijkt dat delen van Amazon in 2050 van koolstofput naar bron kunnen overschakelen  Ons vaderland staat in brand:vrijwilligers sluiten zich aan bij de strijd tegen de bosbranden in Siberië
Ons vaderland staat in brand:vrijwilligers sluiten zich aan bij de strijd tegen de bosbranden in Siberië Meerdere metalen – en mogelijke tekenen van water – gevonden in unieke exoplaneet
Meerdere metalen – en mogelijke tekenen van water – gevonden in unieke exoplaneet Machine learning versnelt de ontdekking van hoogwaardige metaaloxidekatalysatoren
Machine learning versnelt de ontdekking van hoogwaardige metaaloxidekatalysatoren  Wat is een type vulkaan met brede en zachte hellingen gebouwd door de uitbarstingsvloeistofbasalt Lave?
Wat is een type vulkaan met brede en zachte hellingen gebouwd door de uitbarstingsvloeistofbasalt Lave?  meer dan 1, In juli 600 vierkante kilometer Braziliaans Amazonegebied ontbost
meer dan 1, In juli 600 vierkante kilometer Braziliaans Amazonegebied ontbost Kwaliteit lijdt onder rekenkamers die nadruk leggen op niet-auditdiensten, studie toont
Kwaliteit lijdt onder rekenkamers die nadruk leggen op niet-auditdiensten, studie toont
- Elektronica
- Biologie
- Zonsverduistering
- Wiskunde
- French | Italian | Spanish | Portuguese | Swedish | German | Dutch | Danish | Norway |

-
Wetenschap © https://nl.scienceaq.com

