
Wetenschap
Bereken de molaire oplosbaarheid van AGBR in een 3,0 x 10-2 m zilvernitraat AGNO3-oplossing?
1. Begrijp het evenwicht
* Agbr is een spaarzaam oplosbaar zout, wat betekent dat het in een kleine mate in water oplost. De evenwichtsreactie is:
AGBR (S) ⇌ AG⁺ (aq) + br⁻ (aq)
* De oplosbaarheidsproductconstante (KSP) voor AGBR is 5,0 x 10⁻¹³
2. Rekening houden met het gewone ioneneffect
* Zilvernitraat (Agno₃) is een oplosbaar zout dat een gemeenschappelijk ion (Ag⁺) met de AGBR -oplossing biedt. Deze gemeenschappelijke ion zal het evenwicht van de AGBR -oplossing naar links verschuiven, waardoor de oplosbaarheid van AGBR wordt verminderd.
3. Zet een ijstafel op
* We gebruiken een ijs (initiële, verandering, evenwicht) tabel om de concentraties bij te houden.
| | Ag⁺ (M) | Br⁻ (M) |
| ----- | --------- | --------- |
| I | 3.0 x 10⁻² | 0 | (Eerste concentratie van Agno₃)
| C | +S | +S |
| E | 3.0 x 10⁻² + S | S |
* s vertegenwoordigt de molaire oplosbaarheid van AGBR
4. Schrijf de KSP -uitdrukking
* Ksp =[ag⁺] [br⁻] =5,0 x 10⁻¹³
5. Vervangen en oplossen
* Vervang de evenwichtsconcentraties van de ijstafel in de KSP -expressie:
(3,0 x 10⁻² + s) (s) =5,0 x 10⁻¹³
* Omdat de KSP erg klein is, kunnen we aannemen dat S te verwaarlozen is in vergelijking met 3,0 x 10⁻²:
(3.0 x 10⁻²) (s) ≈ 5,0 x 10⁻¹³
* Los op voor s:
S ≈ 5,0 x 10⁻¹³ / 3.0 x 10⁻²
S ≈ 1,7 x 10⁻¹¹ m
Daarom is de molaire oplosbaarheid van AGBR in een zilvernitraatoplossing van 3,0 x 10⁻² m ongeveer 1,7 x 10⁻¹¹ m.
 Welke moleculen hebben een ongelijke lading met meer negatief aan de zijkant en positieve andere?
Welke moleculen hebben een ongelijke lading met meer negatief aan de zijkant en positieve andere?  Kristallen thuis maken voor wetenschappelijke projecten
Kristallen thuis maken voor wetenschappelijke projecten  Berekening van de mate van radicalen
Berekening van de mate van radicalen Hoeveel koper wordt er gewonnen uit het smelten?
Hoeveel koper wordt er gewonnen uit het smelten?  De grondstof die helpt gewrichten te smeren en cellen aan elkaar te binden, is?
De grondstof die helpt gewrichten te smeren en cellen aan elkaar te binden, is?
 Wetenschappers laten zien hoe branden langs waterwegen in de tropische savanne van Australië bedreigde vogels bedreigen
Wetenschappers laten zien hoe branden langs waterwegen in de tropische savanne van Australië bedreigde vogels bedreigen  Hoe reclame zichzelf kan hergebruiken om steden op duurzamere manieren van dienst te zijn
Hoe reclame zichzelf kan hergebruiken om steden op duurzamere manieren van dienst te zijn Disruptieve krachten in het voedselsysteem
Disruptieve krachten in het voedselsysteem Waarom verliezen deeltjes hun aantrekkingskracht en veranderen ze van de ene toestand naar de andere?
Waarom verliezen deeltjes hun aantrekkingskracht en veranderen ze van de ene toestand naar de andere?  Weerrampen in 2020 versterkt door klimaatverandering:rapport
Weerrampen in 2020 versterkt door klimaatverandering:rapport
Hoofdlijnen
- Welke vlinderbloemige boom produceert senna?
- Onderzoek toont aan dat walvissen, al een bedreigde diersoort, kan een vage toekomst tegemoet gaan
- Wat scheidt de cel van zijn omgeving en selecteert wat kan invoeren?
- Geleidelijke opwarming van de aarde culmineerde aan het einde van het Perm in een gigantische uitstervingsgebeurtenis, studievondsten
- Wat is de prominente horizontale banding van organismen die in een bepaalde habitat leven?
- Wiskundig model laat zien hoe een pitadder in het holst van de nacht zijn eten kan vinden
- Welke gasplanten en dieren gebruiken is een product van fotosynthese?
- Nieuw onderzoek wijst uit waarom sommige microbiële genen meer promiscue zijn dan andere
- Hoe een dinosaurus te wegen
- Fladderende vleugels aangedreven door de zon

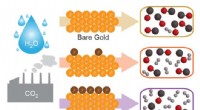
- Wetenschappers stemmen het systeem af om syngas te maken uit CO2
- Onderzoekers ontwikkelen de eerste functionele niet-eigen metaalhydrogenase

- Het beheersen van de nanoschaalstructuur van membranen is essentieel voor schoon water, onderzoekers vinden

- Wat zeekomkommers ons kunnen leren over zelfverdediging

 Wat is de relatie tussen de dichtheid van aardmaterialen en de diepte onder het aardoppervlak?
Wat is de relatie tussen de dichtheid van aardmaterialen en de diepte onder het aardoppervlak?  Luchtvolume berekenen
Luchtvolume berekenen  Wat is een rots aan de top van de klif die plotseling valt?
Wat is een rots aan de top van de klif die plotseling valt?  Wat is de eenheid voor een polair traagheidsmoment?
Wat is de eenheid voor een polair traagheidsmoment?  Definitie van plantenademhaling
Definitie van plantenademhaling
Door fotosynthese transformeren planten zonlicht in potentiële energie in de vorm van de chemische bindingen van koolhydraatmoleculen. Om die opgeslagen energie te gebruiken om hun essentiële levensprocessen te voede
 De normen voor goud en platina instellen waar maar weinigen zijn geweest
De normen voor goud en platina instellen waar maar weinigen zijn geweest Verschillen tussen diepe neurale netwerken en menselijke waarneming
Verschillen tussen diepe neurale netwerken en menselijke waarneming Wat is het verschil tussen een Centriole en een Centrosome?
Wat is het verschil tussen een Centriole en een Centrosome?
- Elektronica
- Biologie
- Zonsverduistering
- Wiskunde
- French | Italian | Spanish | Portuguese | Swedish | German | Dutch | Danish | Norway |

-
Wetenschap © https://nl.scienceaq.com

