
Wetenschap
Welke wordt sneller getolueen of fenol uitgelegd?
Verklaring:
* Activering van de aromatische ring: De hydroxylgroep (-oH) in fenol is een sterk activerende groep, wat betekent dat het de elektronendichtheid van de aromatische ring verhoogt. Dit maakt de ring gevoeliger voor elektrofiele aanval, zoals nitratie.
* Resonantiestabilisatie: Het enige paar elektronen op het zuurstofatoom in fenol kan in de aromatische ring delocaliseren, waardoor resonantiestructuren ontstaan. Deze resonantiestructuren stabiliseren de tussenliggende carbocatie gevormd tijdens nitratie, waardoor de reactie gunstiger wordt.
Nitratiemechanisme:
Nitratie omvat de elektrofiele aanval van een nitroniumion (NO2+) op de aromatische ring. De activerende aard van de hydroxylgroep in fenol maakt de ring meer elektronenrijk en trekt de elektrofiel gemakkelijker aan.
Vergelijking met tolueen:
Tolueen heeft een methylgroep (-CH3), die een zwak activerende groep is. Hoewel de methylgroep de elektronendichtheid van de ring verhoogt, is het effect ervan veel minder uitgesproken dan dat van de hydroxylgroep in fenol.
Conclusie:
Vanwege het sterke activerende effect van de hydroxylgroep en resonantiestabilisatie, wordt fenol veel sneller genitreerd dan tolueen.
 Hoe wordt aardgas geproduceerd uit ruwe olie?
Hoe wordt aardgas geproduceerd uit ruwe olie?  Wat is een natte-bolthermometer?
Wat is een natte-bolthermometer?  Machine-learningsysteem versnelt ontdekking van nieuwe materialen voor 3D-printen
Machine-learningsysteem versnelt ontdekking van nieuwe materialen voor 3D-printen Onderzoekers kweken het meest levensechte bot tot nu toe uit geweven cellen
Onderzoekers kweken het meest levensechte bot tot nu toe uit geweven cellen Hooggeconcentreerde waterige elektrolyten kunnen de in batterijen gebruikte oplosmiddelen vervangen
Hooggeconcentreerde waterige elektrolyten kunnen de in batterijen gebruikte oplosmiddelen vervangen
 Pijpleidingbedrijf bereikt voorlopige schikking in rechtszaken over olieramp in Californië
Pijpleidingbedrijf bereikt voorlopige schikking in rechtszaken over olieramp in Californië Boeren of verzamelaars? De prekoloniale voedselproductie van de Aboriginals was nauwelijks zo eenvoudig
Boeren of verzamelaars? De prekoloniale voedselproductie van de Aboriginals was nauwelijks zo eenvoudig  Hoe insecten insecten bestuiven?
Hoe insecten insecten bestuiven?  Foto's laten zien dat de ongrijpbare boshond wijdverbreid is in Panama
Foto's laten zien dat de ongrijpbare boshond wijdverbreid is in Panama  Paleontologen ontdekken solide bewijs van voorheen ongrijpbare abrupte sprong op zeeniveau
Paleontologen ontdekken solide bewijs van voorheen ongrijpbare abrupte sprong op zeeniveau
Hoofdlijnen
- Wat eten Lotis Blue Butterflies?
- Wat wordt gebruikt om aan te tonen dat het DNA -molecuul een helix?
- Mijnstudie laat zien hoe snel bacteriën kunnen evolueren
- Er wordt een verrassende nieuwe vlindervis beschreven uit de Filippijnse schemerzone en tentoonstelling
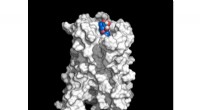
- Structuur van primaire optogenetische tool onthuld
- Wat is het verschil tussen cytoplasma en protoplasma?
- Hoe verschilt eiwitsynthese in prokaryoten en eukaryote?
- De celstructuur van een ui
- Wie was de eerste wetenschapper die cellen zag?
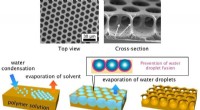
- Uit de mist:Honingraatfilms
- Een eenvoudige methode ontwikkeld voor 3D-biofabricage op basis van bacteriële cellulose

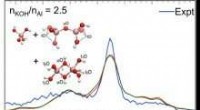
- Aluminiumcomplexen geïdentificeerd via vibrationele vingerafdrukken
- Wetenschappers stellen een nieuwe strategie voor om het celcommunicatienetwerk te reguleren

- Laatste bevindingen over bittere stoffen in koffie
 Drie manieren om een neolithische vindplaats te behouden
Drie manieren om een neolithische vindplaats te behouden Uit onderzoek blijkt dat de stabiliteit van de wateropbrengst in stroomgebieden afneemt
Uit onderzoek blijkt dat de stabiliteit van de wateropbrengst in stroomgebieden afneemt  Hoe lichaamspantser werkt
Hoe lichaamspantser werkt  Hoeveel straling geeft een computertransformator af?
Hoeveel straling geeft een computertransformator af?  Ja, AI kan sommige banen in beslag nemen, maar het kan ook betekenen dat meer mannen in de zorg werken
Ja, AI kan sommige banen in beslag nemen, maar het kan ook betekenen dat meer mannen in de zorg werken Hoe planten en dieren interageren in het regenwoud
Hoe planten en dieren interageren in het regenwoud Ik heb het gedaan:Portugese hacker zegt dat hij Afrikaanse tycoon heeft ontmaskerd
Ik heb het gedaan:Portugese hacker zegt dat hij Afrikaanse tycoon heeft ontmaskerd Wat is een ingestorte ster?
Wat is een ingestorte ster?
- Elektronica
- Biologie
- Zonsverduistering
- Wiskunde
- French | Italian | Spanish | Portuguese | Swedish | German | Dutch | Danish | Norway |

-
Wetenschap © https://nl.scienceaq.com

