
Wetenschap
Een chemicus lost 3,50 g kaliumjodaat en 6,23 hydroxide in 805,05 water op Wat is de percentage concentratie elke opgeloste oplossing?
Inzicht in de percentage concentratie
Percentageconcentratie (ook bekend als massa/volumepercentage) drukt de hoeveelheid opgeloste stof (in gram) uit opgelost in 100 ml oplossing.
Berekeningen
1. Totale oplossingmassa:
* Massa kaliumjodaat (ki) =3,50 g
* Massa kaliumhydroxide (KOH) =6,23 g
* Mass van water (H₂o) =805,05 g
* Totale oplossingmassa =3,50 g + 6,23 g + 805,05 g =814,78 g
2. Percentage concentratie kaliumjodaat:
* (Massa ki / totale massa oplossing) * 100%
* (3,50 g / 814,78 g) * 100% = 0,43%
3. Percentage concentratie kaliumhydroxide:
* (Massa KOH / totale oplossingmassa) * 100%
* (6,23 g / 814,78 g) * 100% = 0,76%
Belangrijke opmerking: De oplossing is waarschijnlijk erg verdund vanwege de grote hoeveelheid water.
Laat het me weten als je de concentratie in verschillende eenheden wilt berekenen (zoals molariteit of molaliteit)!
 Welke planten groeien het beste in City Garden?
Welke planten groeien het beste in City Garden?  Europa zindert in hittegolf terwijl bosbrand Portugal treft (update)
Europa zindert in hittegolf terwijl bosbrand Portugal treft (update) Amerikaanse zeearenden eten prairiehonden? Onderzoekers onderstrepen de relatie tussen roofvogels en knaagdieren in de Great Plains
Amerikaanse zeearenden eten prairiehonden? Onderzoekers onderstrepen de relatie tussen roofvogels en knaagdieren in de Great Plains  Eerste ontdekking van microplastics uit water dat vastzit op bladeren van planten
Eerste ontdekking van microplastics uit water dat vastzit op bladeren van planten Uit onderzoek blijkt dat dezelfde voedingsmiddelen een duidelijk verschillende impact op het milieu hebben
Uit onderzoek blijkt dat dezelfde voedingsmiddelen een duidelijk verschillende impact op het milieu hebben
Hoofdlijnen
- In sommige delen van de VS daalt het aantal wilde kalkoenen; de belangrijkste reden kan het verlies van leefgebied zijn
- Orka's migreren, studievondsten, maar waarom?
- Wat is perifeer bloed?
- Welke theorie verklaart waarom de populatie in de loop van de tijd kan worden gewijzigd?
- Wat is het voedsel dat door een plant is opgeslagen in de vorm van suiker of zetmeel?
- Welk type organisme is een natuurlijke selectie van leeuwen of selectief fokken?
- Klein maar krachtig:plankton behoort tot de krachtigste wezens op aarde
- Wat gebeurt er met een dierlijke cel in zuiver water? Waarom gebeurt dit niet bij een plantencel?
- Wat is anaëroob?
- Nieuwe methode kan op efficiënte wijze verschillende bouwstenen van farmaceutische medicijnen creëren
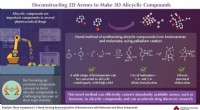
- Onderzoekers lossen een wetenschappelijk mysterie over verdamping op

- Kunststof van hout? Röntgenanalyse wijst de weg naar op lignine gebaseerde componenten op maat
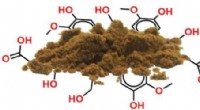
- Bakstenen bouwen van plastic afval

- Het volgen van eiwitverwijdering kan leiden tot verbeterde therapieën

 Waarom landen astronauten aan de donkere kant van de maan?
Waarom landen astronauten aan de donkere kant van de maan?  Hoe wordt energie overgedragen van de zon naar aarde en atmosfeer?
Hoe wordt energie overgedragen van de zon naar aarde en atmosfeer?  Welke wordt gebruikt voor zuurstoftransport in levende organismen?
Welke wordt gebruikt voor zuurstoftransport in levende organismen?  Waarom zijn bladeren afwezig in cactus?
Waarom zijn bladeren afwezig in cactus?  Als een overmaat stikstof wordt omgezet met 3,41 gram waterstof, hoeveel ammoniak kan er dan ontstaan?
Als een overmaat stikstof wordt omgezet met 3,41 gram waterstof, hoeveel ammoniak kan er dan ontstaan?  Duurzaam, hoogwaardig papiercoatingmateriaal zou de vervuiling door microplastic kunnen verminderen
Duurzaam, hoogwaardig papiercoatingmateriaal zou de vervuiling door microplastic kunnen verminderen  Wat is het kleinste deel van een compound die de eigenschapsmaatschappij behoudt?
Wat is het kleinste deel van een compound die de eigenschapsmaatschappij behoudt?  Waar wordt zonne -energie voor gebruikt?
Waar wordt zonne -energie voor gebruikt?
- Elektronica
- Biologie
- Zonsverduistering
- Wiskunde
- French | Italian | Spanish | Portuguese | Swedish | German | Dutch | Danish | Norway |

-
Wetenschap © https://nl.scienceaq.com

