
Wetenschap
Als een 12,8 g natriummonster volledig reageert met 19,6 g chloor om 32,4 chloride te vormen, zijn deze chemische veranderingen consistent de wet voor het behoud van de wet?
Ja, de chemische veranderingen zijn consistent met de wet van behoud van massa. Dit is waarom:
De wet van behoud van massa
De wet van behoud van massa stelt dat in een gesloten systeem de totale massa van de reactanten vóór een chemische reactie gelijk moet zijn aan de totale massa van de producten na de reactie.
analyse
* reactanten:
* Natrium (NA):12,8 g
* Chloor (CL2):19,6 g
* Totale massa reactanten:12,8 g + 19,6 g =32,4 g
* Product:
* Natriumchloride (NaCl):32,4 g
Conclusie
De totale massa van de reactanten (32,4 g) is gelijk aan de totale massa van het product (32,4 g). Dit bevestigt dat de chemische reactie zich hecht aan de wet van behoud van massa.
 Hoe het niet-polaire karakter van oliemoleculen helpt bij het verwijderen uit water?
Hoe het niet-polaire karakter van oliemoleculen helpt bij het verwijderen uit water?  Wat is het doel van het toevoegen van NaCl -oplossing aan zeepmengsel?
Wat is het doel van het toevoegen van NaCl -oplossing aan zeepmengsel?  Hoeveel natuurlijke voorkomende stoffen zijn er die niet door chemicaliën kunnen worden opgesplitst in eenvoudigere stoffen?
Hoeveel natuurlijke voorkomende stoffen zijn er die niet door chemicaliën kunnen worden opgesplitst in eenvoudigere stoffen?  Welke goede dingen doet de ozone?
Welke goede dingen doet de ozone?  Waar gebruiken mensen zwavel voor?
Waar gebruiken mensen zwavel voor?
 Waterkrachtdammen koelen rivieren in het stroomgebied van de Mekong, satellieten tonen
Waterkrachtdammen koelen rivieren in het stroomgebied van de Mekong, satellieten tonen Wat is habitat?
Wat is habitat?  Wat zijn de kenmerken van sprinkhanen?
Wat zijn de kenmerken van sprinkhanen?  Beperk klimaatverandering op een gemakkelijke manier:hak geen grote bomen om
Beperk klimaatverandering op een gemakkelijke manier:hak geen grote bomen om Mars trekt aan:hoe de interacties van de aarde met de rode planeet de diepzeecirculatie stimuleren
Mars trekt aan:hoe de interacties van de aarde met de rode planeet de diepzeecirculatie stimuleren
Hoofdlijnen
- Bacteriën en virussen infecteren onze cellen via suikers:nu willen onderzoekers weten hoe ze dat doen
- Weten wat je moet bewaren en weggooien:hoe een enzym cellulaire berichten onderscheidt
- Wat is tamme gist?
- Welke verklaring beschrijft een wetenschappelijke theorie?
- Nieuwe aanpak kan de sleutel zijn tot de behandeling van antibioticaresistente bacteriën
- Welk domein multicellulaire fotosynthetische organismen?
- De circadiane klok bepaalt het tempo van de plantengroei
- Kevers felle kleuren gebruikt voor camouflage in plaats van roofdieren te waarschuwen
- Wetenschappers ontcijferen hoe planten zonnebrand voorkomen
- Wetenschappers onthullen structurele geheimen van baleinwalvissen

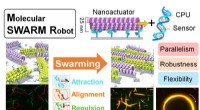
- Wetenschappers werken eraan om robots ter grootte van een molecuul samen te laten zwermen om taken uit te voeren
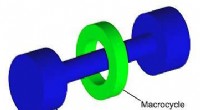
- Onderzoekers maken 's werelds snelste moleculaire shuttle
- Chemici ontwerpen mini-ecosystemen om de werking van medicijnen te testen

- Nieuwe studie levert bewijs voor decennia-oude theorie om het vreemde gedrag van water te verklaren

 Wat zijn III-groepselementen in het periodiek systeem?
Wat zijn III-groepselementen in het periodiek systeem?  Onafhankelijke voogden hebben een impact op jonge overlevenden van kinderhandel
Onafhankelijke voogden hebben een impact op jonge overlevenden van kinderhandel  Waar komt het chemische symbool van helium vandaan?
Waar komt het chemische symbool van helium vandaan?  Is CO2 en olie gemengd gevaarlijk?
Is CO2 en olie gemengd gevaarlijk?  Grondwaterafvoer beïnvloedt de waterkwaliteit in kustwateren
Grondwaterafvoer beïnvloedt de waterkwaliteit in kustwateren Egelaanpassing
Egelaanpassing  Diamanten maken gebruik van zowel optische microscopie als MRI voor betere beeldvorming
Diamanten maken gebruik van zowel optische microscopie als MRI voor betere beeldvorming Renault kijkt actief naar de toekomst na Ghosn
Renault kijkt actief naar de toekomst na Ghosn
- Elektronica
- Biologie
- Zonsverduistering
- Wiskunde
- French | Italian | Spanish | Portuguese | Swedish | German | Dutch | Danish | Norway |

-
Wetenschap © https://nl.scienceaq.com

