
Wetenschap
Is RB F a ionische of covalente binding?
* Elektronegativiteitsverschil: Rubidium (RB) is een metaal met een lage elektronegativiteit, terwijl fluor (F) een zeer elektronegatief niet -metaal is. Het verschil in elektronegativiteit tussen hen is significant, wat leidt tot de overdracht van een elektron van rubidium naar fluor.
* Vorming van ionen: Rubidium verliest één elektron om een positief geladen ion (RB+) te worden, terwijl fluor één elektron krijgt om een negatief geladen ion te worden (F-).
* Elektrostatische aantrekkingskracht: De tegengesteld geladen ionen trekken elkaar sterk aan en vormen een ionische binding.
Samenvattend: Het grote elektronegativiteitsverschil tussen rubidium en fluor resulteert in de vorming van ionen en hun elektrostatische aantrekkingskracht, kenmerkend voor een ionische binding.
 Wat is de mooiste bug op aarde?
Wat is de mooiste bug op aarde?  Hoe het leven in de stratosfeer ons leert over de mogelijkheid van extremen op andere werelden
Hoe het leven in de stratosfeer ons leert over de mogelijkheid van extremen op andere werelden  Nieuwe aanpak om gifstoffen uit afvalwater te verwijderen
Nieuwe aanpak om gifstoffen uit afvalwater te verwijderen Vervuilingsniveaus van waas vertonen kortstondig wipgedrag boven Noord-Chinese vlakte
Vervuilingsniveaus van waas vertonen kortstondig wipgedrag boven Noord-Chinese vlakte Onderzoekers werken aan systematische beoordeling van klimaatmodellen
Onderzoekers werken aan systematische beoordeling van klimaatmodellen
Hoofdlijnen
- Wat betekent kolonies?
- Wat maakt een held?
- Wat dient niet als een site voor de productie van bloedcellen in de zich ontwikkelende foetus?
- Wat is de tweedeling van botten?
- Wetenschappers vinden ontbrekende aanwijzing over hoe hiv cellen hackt om zichzelf te verspreiden
- Welke organismen hebben vier kamer met een kamer?
- Computersimulatie laat zien hoe de evolutie mogelijk is versneld
- Hoe rouw werkt
- Wat zijn resultaten in de wetenschap?
- Onderzoekers ontwikkelen groene alternatieven voor fossiele grondstoffen

- Milieuvriendelijke chemicaliën kunnen de verwerking van mineralen zelfs verbeteren

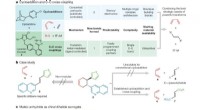
- Het beste van twee werelden:twee skeletvormende chemische reacties combineren
- Middeleeuwse kruitrecepten opblazen

- De wolken van spaghetti die DNA-gegevens veilig houden
 Wat is het tegenovergestelde van homozygote dominant?
Wat is het tegenovergestelde van homozygote dominant?  Welk gebied in Oklahoma is zo dicht dat het als een barrière tussen oosterse en westerse staat is?
Welk gebied in Oklahoma is zo dicht dat het als een barrière tussen oosterse en westerse staat is?  Hoe is wiskunde betrokken bij het worden van een apotheker?
Hoe is wiskunde betrokken bij het worden van een apotheker?  Het koppelsimulatiemodel van psychologieprofessoren helpt ons in de mysteries van partnerselectie te duiken
Het koppelsimulatiemodel van psychologieprofessoren helpt ons in de mysteries van partnerselectie te duiken Wat zijn de belangrijkste verschillen tussen plantencellen en dierlijke cellen?
Wat zijn de belangrijkste verschillen tussen plantencellen en dierlijke cellen?  Vreemde aardbeving onthult verborgen mechanisme
Vreemde aardbeving onthult verborgen mechanisme ANU nodigt burgerwetenschappers uit om naar exploderende sterren te zoeken
ANU nodigt burgerwetenschappers uit om naar exploderende sterren te zoeken Nieuw op digitale camera's gebaseerd systeem kan om de hoek kijken
Nieuw op digitale camera's gebaseerd systeem kan om de hoek kijken
- Elektronica
- Biologie
- Zonsverduistering
- Wiskunde
- French | Italian | Spanish | Portuguese | Swedish | German | Dutch | Danish | Norway |

-
Wetenschap © https://nl.scienceaq.com

