
Wetenschap
Wat is de netto ionische vergelijking voor Na H2O?
* Natrium (NA) reageert met water (H₂o): Natrium is een zeer reactief alkalimetaal. Wanneer het reageert met water, produceert het natriumhydroxide (NaOH) en waterstofgas (H₂). De reactie is krachtig en exotherme.
* De gebalanceerde chemische vergelijking:
2 NA (S) + 2 H₂o (L) → 2 NaOH (AQ) + H₂ (G)
* ionische vergelijking:
2 Na (s) + 2 H₂o (L) → 2 Na⁺ (aq) + 2 oh⁻ (aq) + h₂ (g)
* Netto ionische vergelijking:
2 Na (s) + 2 H₂o (L) → 2 Na⁺ (aq) + 2 oh⁻ (aq) + h₂ (g)
Verklaring:
* In deze reactie is natrium (NA) een vaste stof en bestaat het niet als ionen in oplossing.
* Water (H₂o) is een vloeistof en dissocieert niet volledig in ionen.
* Natriumhydroxide (NaOH) is een sterke basis en dissocieert volledig in NA⁺ en OH⁻ -ionen in oplossing.
* Waterstofgas (H₂) is een gas en bestaat niet als ionen.
Daarom zijn alle soorten in de reactie betrokken bij de netto ionische vergelijking , en er zijn geen toeschouwersionen om uit te annuleren.
 Stedelijke luchtvervuiling – wat zijn de belangrijkste bronnen over de hele wereld?
Stedelijke luchtvervuiling – wat zijn de belangrijkste bronnen over de hele wereld?  Video:Hoe zullen kuststeden zich aanpassen aan de stijging van de zeespiegel?
Video:Hoe zullen kuststeden zich aanpassen aan de stijging van de zeespiegel?  Over heersende Westerlies
Over heersende Westerlies Wat zijn de kenmerken van overstromingen?
Wat zijn de kenmerken van overstromingen?  Droefheid, walging, woede:angst voor het Great Barrier Reef maakte klimaatverandering urgent
Droefheid, walging, woede:angst voor het Great Barrier Reef maakte klimaatverandering urgent
Hoofdlijnen
- Waarom is nomenclatuur belangrijk?
- Toyocamycine-opnamewijze ontdekt:goed nieuws voor de ontwikkeling van antischimmelmiddelen
- Wat zijn fysiometrie?
- Welke vissen zijn omnivoren?
- Welk systeem is meer geavanceerd bij cnidarians dan Porifera?
- Welk deel van neuron vrijgeven of chemische boodschappers sturen?
- Wat zijn twee voorbeelden van aminozuren?
- Welk celtype is de geleidende cel van het zenuwstelsel?
- Zullen geavanceerde organismen hetzelfde zijn als complexe organismen, waarom?
- Vaccin-ingrediënten kunnen zich verbergen in bibliotheken met kleine moleculen
- Ideale methode voor het snel testen van ziekten

- AI-aangedreven elektronische neus om de versheid van vlees te ruiken

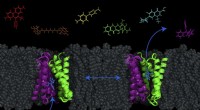
- Nieuw model onthult mogelijkheid om antibiotica in bacteriën te pompen
- Modern poreus materiaal lijkt op XIV-eeuws Alhambra-mozaïek

 Verbeterde secundaire waas door emissiereductie tijdens COVID-19-lockdown in China
Verbeterde secundaire waas door emissiereductie tijdens COVID-19-lockdown in China Wat zijn enkele niet-voorbeelden van eiwitten?
Wat zijn enkele niet-voorbeelden van eiwitten?  Welke stoffen in de lucht zijn elementen?
Welke stoffen in de lucht zijn elementen?  Effecten van zichtbare lichtstraling
Effecten van zichtbare lichtstraling  Oorzaak versus correlatie uitgelegd met 10 voorbeelden
Oorzaak versus correlatie uitgelegd met 10 voorbeelden  Waar is het Jefferson Monument?
Waar is het Jefferson Monument?  Een mijlpaal op weg naar efficiënte zonnecellen
Een mijlpaal op weg naar efficiënte zonnecellen Juiste manier om een grafiek te labelen
Juiste manier om een grafiek te labelen
- Elektronica
- Biologie
- Zonsverduistering
- Wiskunde
- French | Italian | Spanish | Portuguese | Swedish | German | Dutch | Danish | Norway |

-
Wetenschap © https://nl.scienceaq.com

