
Wetenschap
Wat is de aard van p o binding in fosfor pentoxide p2O5?
* Elektronegativiteitsverschil: Zuurstof is elektronegatiefer dan fosfor. Dit betekent dat zuurstof een sterkere aantrekkingskracht heeft voor de gedeelde elektronen in de binding, wat leidt tot een gedeeltelijke negatieve lading (Δ-) op het zuurstofatoom en een gedeeltelijke positieve lading (δ+) op het fosforatoom.
* ionisch karakter: Het grote elektronegativiteitsverschil tussen fosfor en zuurstof draagt bij aan een significant ionisch karakter in de P-O-binding. Dit betekent dat de elektronen in de binding niet gelijk worden gedeeld, maar nauwer worden geassocieerd met het zuurstofatoom.
* Polaire covalente binding: Hoewel het ionische karakter significant is, omvat de P-O-binding nog steeds het delen van elektronen, waardoor het een polaire covalente binding is.
Structuur van P₂o₅:
P₂o₅ bestaat in verschillende vormen, maar de meest voorkomende is de tetrahedral p₄o₁₀ . Dit molecuul bestaat uit vier fosforatomen, elk gebonden aan vier zuurstofatomen in een tetraëdrische opstelling. De zuurstofatomen zijn gerangschikt op een manier die twee soorten P-O-bindingen creëert:
* p =o: Dit zijn dubbele bindingen en zijn korter en sterker dan de P-O enkele bindingen.
* P-O-P: Dit zijn enkele bindingen die de fosforatomen verbinden.
Belangrijke opmerking: Het significante ionische karakter in de P-O-binding draagt bij aan de zeer reactieve aard van fosfor pentoxide. Het reageert gemakkelijk met water om fosforzuur te vormen (H₃po₄), een sterk zuur.
 Evenwichtige vergelijking van koper- en zilvernitraat?
Evenwichtige vergelijking van koper- en zilvernitraat?  Hoe de netto ionische vergelijking voor CH3COOH te schrijven terwijl deze met NaOH reageert
Hoe de netto ionische vergelijking voor CH3COOH te schrijven terwijl deze met NaOH reageert  Dichtheid versus concentratie
Dichtheid versus concentratie  Een katalysator voor elektronisch gestuurde C-H-functionalisatie
Een katalysator voor elektronisch gestuurde C-H-functionalisatie  Ingenieurs ontwikkelen botachtig metaalschuim dat bij kamertemperatuur kan worden genezen
Ingenieurs ontwikkelen botachtig metaalschuim dat bij kamertemperatuur kan worden genezen
Hoofdlijnen
- Waarin verschillen vaatplanten van niet-vaatplanten?
- Wat gebruik je bij het meten van elektroforese?
- Wat zijn manieren waarop aerobe en anaërobe ademhaling vergelijkbaar zijn?
- Nugget the cow:Zeewier-kauwend rund kauwt op oplossing voor methaanprobleem
- Gletsjermuizen bewegen en dat heeft wetenschappers versteld doen staan
- Onder de microscoop gespot:hoe een virus zijn pantser aantrekt
- Waarom is replicatie belangrijk in de wetenschap?
- Koala's hebben een vreemd dieet:zijn het bacteriën?
- Hoe kan een verandering in het polypeptide de celactiviteit beïnvloeden?
- Chemici bereiken belangrijke mijlpaal van synthese:chirale inductie op afstand
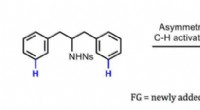
- MOF-cokatalysator maakt selectiviteit van vertakte aldehyden tot 90% mogelijk

- Een kwestie van mobiliteit:multidisciplinair artikel suggereert nieuwe strategie voor medicijnontdekking
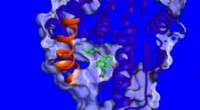
- Betere metaaloxiden om de groene eigenschappen van veel energietoepassingen te stimuleren
- Onderzoekers bedenken kleine, hersluitbare pakketten om materialen op tijd af te leveren

 Katalysatorvervroeging verwijdert verontreinigende stoffen bij lage temperaturen
Katalysatorvervroeging verwijdert verontreinigende stoffen bij lage temperaturen Singlet-zuurstof breekt selectief oxytetracycline af in fenton-achtige oxidatie
Singlet-zuurstof breekt selectief oxytetracycline af in fenton-achtige oxidatie Voedselzekerheid bedreigd door zeespiegelstijging
Voedselzekerheid bedreigd door zeespiegelstijging Waarom zijn tuinen aardvriendelijk?
Waarom zijn tuinen aardvriendelijk?  Welke kracht van aantrekkingskracht is verantwoordelijk voor de vorming een dunne film op oppervlaktewater?
Welke kracht van aantrekkingskracht is verantwoordelijk voor de vorming een dunne film op oppervlaktewater?  Wat is de wederkerige van een getal?
Wat is de wederkerige van een getal?  Wat is een voorbeeld van een onevenwichtig ecosysteem in de oceaan?
Wat is een voorbeeld van een onevenwichtig ecosysteem in de oceaan?  Onderzoekers bepalen hoe type II restrictie-endonuclease Sau3AI DNA splitst
Onderzoekers bepalen hoe type II restrictie-endonuclease Sau3AI DNA splitst
- Elektronica
- Biologie
- Zonsverduistering
- Wiskunde
- French | Italian | Spanish | Portuguese | Swedish | German | Dutch | Danish | Norway |

-
Wetenschap © https://nl.scienceaq.com

