
Wetenschap
Wat gebeurt er als de elementen fosfor een ion vormen?
de natuurlijke neiging van Phosphorus
* Fosfor (P) bevindt zich in groep 15 (VA) van het periodiek systeem, ook bekend als de PNICTOGENS.
* Het heeft 5 valentie -elektronen (elektronen in de buitenste schaal).
* Om een stabiel octet (8 elektronen) te bereiken, zoals de edelgassen, wil Phosporus nog 3 elektronen krijgen.
Vorming van een fosfide -ion
* Wanneer fosfor 3 elektronen wint, wordt het een negatief geladen ion genaamd een fosfide -ion , voorgesteld als p³⁻ .
* Deze versterking van elektronen creëert een stabiele configuratie met 8 valentie -elektronen, waardoor het iso -elektronisch is (met hetzelfde aantal elektronen) met het edelgasargon.
Key Points
* ionische verbindingen: Fosfide -ionen combineren meestal met positief geladen ionen (kationen) om ionische verbindingen te vormen. Natriumfosfide (Na₃P) ontstaat bijvoorbeeld wanneer drie natriumionen (Na⁺) binding met één fosfide -ion (p³⁻).
* Covalente bindingen: Fosfor kan ook covalente bindingen vormen met andere niet -metalen, waarbij elektronen worden gedeeld om een stabiel octet te bereiken.
Laat het me weten als je meer details wilt over specifieke fosfor-bevattende verbindingen!
 Wat zouden de beste hulpmiddelen zijn om de dichtheid van een klein zilvererts te meten?
Wat zouden de beste hulpmiddelen zijn om de dichtheid van een klein zilvererts te meten?  Video:Waarom plastic flessen worden gerecycled tot kleding
Video:Waarom plastic flessen worden gerecycled tot kleding Verfijnen hoe olie werkt
Verfijnen hoe olie werkt  Wat is de chemische naam van het eten van zout?
Wat is de chemische naam van het eten van zout?  Hoogrenderende katalysator verbetert de elektrische reductieprestaties van kooldioxide
Hoogrenderende katalysator verbetert de elektrische reductieprestaties van kooldioxide
 Onderzoek toont snelle zeespiegelstijging langs de Atlantische kust van Noord-Amerika in de 18e eeuw
Onderzoek toont snelle zeespiegelstijging langs de Atlantische kust van Noord-Amerika in de 18e eeuw Kunnen aardwarmteprojecten aardbevingen veroorzaken?
Kunnen aardwarmteprojecten aardbevingen veroorzaken?  Hoe het leven in de stratosfeer ons leert over de mogelijkheid van extremen op andere werelden
Hoe het leven in de stratosfeer ons leert over de mogelijkheid van extremen op andere werelden  Werelds transitie naar schone energie te traag:IEA
Werelds transitie naar schone energie te traag:IEA De helft van China getroffen door droogte tijdens ergste hittegolf ooit
De helft van China getroffen door droogte tijdens ergste hittegolf ooit
Hoofdlijnen
- Hoeveel chromosomen zijn er in een cel die is gevormd uit sperma- en eiercel?
- Onderzoekers ontdekken een parallel universum in de tomatengenetica
- Wat betekenen de gegevens in een wetenschappelijk project?
- Wat werken de verschillende soorten bloedcellen samen om immuunrespons te produceren?
- Wat is een Alektropia?
- Verschillen cytokinese in plantencellen en dierlijke cellen?
- Wat gebruiken wetenschappers hulpmiddelen?
- Welke organel speelt de belangrijkste rol in de fotosynthese?
- Wat is het enzymatische mechanisme voor RNA -splitsing?
- Weer een stap dichter bij afstembare vloeistoffen
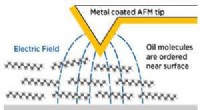
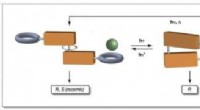
- Een moleculaire motor gebruiken om de voorkeur van anionbindende katalysatoren te veranderen
- Contacttraceersysteem voor blootstelling aan chemische stoffen in het milieu

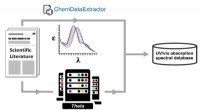
- Automatische aanmaak van databases voor materiaalontdekking:innovatie uit frustratie
- Bacteriedodend glas biedt hoop in strijd tegen ziekenhuisinfecties

 Wat is een kenmerk dat bloed anders maakt dan enig ander weefsel?
Wat is een kenmerk dat bloed anders maakt dan enig ander weefsel?  Quantum dots bieden volledige controle over fotonen
Quantum dots bieden volledige controle over fotonen De manier waarop stimuleringsdollars worden uitgegeven, zal de uitstoot decennialang beïnvloeden
De manier waarop stimuleringsdollars worden uitgegeven, zal de uitstoot decennialang beïnvloeden  Wiskundigen stellen een nieuwe manier voor om neurale netwerken te gebruiken om te werken met lawaaierige, hoogdimensionale gegevens
Wiskundigen stellen een nieuwe manier voor om neurale netwerken te gebruiken om te werken met lawaaierige, hoogdimensionale gegevens Nieuw bubbelmechanisme ontdekt in de natuurkunde
Nieuw bubbelmechanisme ontdekt in de natuurkunde Welke eigenschap hebben vloeistoffen en gassen gemeen?
Welke eigenschap hebben vloeistoffen en gassen gemeen?  Welk type verwering zorgt ervoor dat de minerale samenstellingsrots verandert?
Welk type verwering zorgt ervoor dat de minerale samenstellingsrots verandert?  Waarom zijn deze attitudes belangrijk in de studie en de praktijk van de wetenschap?
Waarom zijn deze attitudes belangrijk in de studie en de praktijk van de wetenschap?
- Elektronica
- Biologie
- Zonsverduistering
- Wiskunde
- French | Italian | Spanish | Portuguese | Swedish | German | Dutch | Danish | Norway |

-
Wetenschap © https://nl.scienceaq.com

