
Wetenschap
Het aantal zwavelatomen in moleculaire zwavel van 27,1 g?
1. Bepaal de moleculaire formule van zwavel
* Moleculaire zwavel bestaat als een ring van acht zwavelatomen, weergegeven door de formule S₈.
2. Bereken de molaire massa van S₈
* De atoommassa van zwavel (s) is ongeveer 32,07 g/mol.
* De molaire massa van S₈ is 32,07 g/mol * 8 =256,56 g/mol
3. Converteer gram van S₈ naar mol
* Verdeel de gegeven massa zwavel (27,1 g) door de molaire massa van S₈:
27.1 g / 256,56 g / mol =0,1056 mol S₈
4. Bereken het aantal zwavelatomen
* Vermenigvuldig het aantal mol S₈ met Avogadro's nummer (6.022 x 10²³ atomen/mol) en met het aantal zwavelatomen per S₈ -molecuul (8):
0.1056 Mol S₈ * 6.022 x 10²³ Atomen/mol * 8 Atomen/Molecule = 5,09 x 10²³ Zwavelatomen
Daarom zijn er ongeveer 5,09 x 10²³ zwavelatomen in 27,1 g moleculaire zwavel.
 Superdichte pakking van waterstofmoleculen op een oppervlak
Superdichte pakking van waterstofmoleculen op een oppervlak Noem 10 dingen gemaakt van steenkool?
Noem 10 dingen gemaakt van steenkool?  Waarom is natrium verpakt in polythene?
Waarom is natrium verpakt in polythene?  Als kalksteen werd verpletterd, wat zou het dan doen met de reactiesnelheid tussen een zuur en kalksteen?
Als kalksteen werd verpletterd, wat zou het dan doen met de reactiesnelheid tussen een zuur en kalksteen?  Wat vertelt u hoeveel atomen van een reactant of product deelnemen aan reactie?
Wat vertelt u hoeveel atomen van een reactant of product deelnemen aan reactie?
Hoofdlijnen
- Wat is een positieve controle in de microbiologie?
- Waarom groeit de groei vanuit het midden van het lichaam naar buiten?
- Onafhankelijk en afhankelijk zijn dit soorten in de wetenschap?
- Hoe hersenspoeling werkt
- Waarom wordt beperkingsenzym ook Endonuclease -enzym genoemd?
- Welke dieren vertoont geen segmentatie en menselijke wezens B-aardewormen C-insecten D-kwallen?
- Hoe groeit een organisme?
- Designer-eiwitten die genetisch materiaal verpakken, kunnen helpen bij het leveren van gentherapie
- Wat is de intermembrale index van de mens?
- Wat maakt kobalt essentieel voor het leven?

- Een vleugje goud stuurt kristallen elektrisch van opwinding

- Model voor op 2D materiaal gebaseerde RRAM gevonden

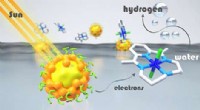
- Goedkoper, minder giftige en recyclebare lichtabsorbers voor waterstofproductie
- Moleculaire additieven verbeteren de mechanische eigenschappen van organisch zonnecelmateriaal

 Lichtgestuurd stroomtransport door geladen atomen voor het eerst gedemonstreerd
Lichtgestuurd stroomtransport door geladen atomen voor het eerst gedemonstreerd De hittegolf in Californië zorgt voor stroomonderbrekingen, brandgevaar
De hittegolf in Californië zorgt voor stroomonderbrekingen, brandgevaar Hoe werken trick-verjaardagskaarsen?
Hoe werken trick-verjaardagskaarsen?  Nieren genezen met nanotechnologie
Nieren genezen met nanotechnologie Wat inktvisneuronen en een octopus in extase ons over onszelf kunnen leren
Wat inktvisneuronen en een octopus in extase ons over onszelf kunnen leren  Reiken verder dan het normale bewegingsbereik?
Reiken verder dan het normale bewegingsbereik?  Machine learning gebruiken voor het ontdekken van muziekkennis
Machine learning gebruiken voor het ontdekken van muziekkennis Bionanotechnologie heeft een nieuw gezicht, toekomst van wereldklasse
Bionanotechnologie heeft een nieuw gezicht, toekomst van wereldklasse
- Elektronica
- Biologie
- Zonsverduistering
- Wiskunde
- French | Italian | Spanish | Portuguese | Swedish | German | Dutch | Danish | Norway |

-
Wetenschap © https://nl.scienceaq.com

